题目内容
| A、Na2O2晶体中阴阳离子个数之比为1:1 | B、Na2O2晶体中既有离子键又有非极性共价键 | C、Na2O2在空气中加热可以得到更稳定的Na2O | D、Na2O2长期露置于空气中最终转变成NaOH |
B.一般金属元素与非金属元素形成离子键,同种非金属元素之间形成非极性键,不同种非金属元素之间形成极性共价键;
C.Na2O2比Na2O稳定;
D.Na2O2易与水反应生成NaOH,NaOH吸收空气中的水和CO2生成Na2CO3?xH2O,Na2CO3?xH2O风化脱水生成Na2CO3.
B.过氧化钠中钠离子和过氧根离子间存在离子键,过氧根离子中氧原子和氧原子之间存在非极性共价键,故B正确;
C.Na2O2比Na2O稳定,所以Na2O在空气中加热可以得到更稳定的Na2O2,故C错误;
D.Na2O2易与水反应生成NaOH,NaOH吸收空气中的水和CO2生成Na2CO3?xH2O,Na2CO3?xH2O风化脱水生成Na2CO3,故D错误;
故选B.

 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案(12分)某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动。
【提出问题】这种淡黄色粉末是什么?有什么性质和用途?
【查阅资料】①硫是淡黄色粉末,不溶于水;②过氧化钠(Na2O2)是淡黄色粉末,在常温下能与水反应生成碱和一种气体;在呼吸面具中和潜水艇里常用作供氧剂。
【猜想与探究】猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物。
探究:过氧化钠与水反应的生成物的成分。
【实验与结论】
| | 实验操作 | 实验现象 | 实验结论 |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水 | _____________________ | 猜想a、c不成立,猜想b成立。 |
| 探究 | ①用带火星的木条伸入过氧化钠与水反应的试管中 | 木条复燃 | 生成物有___________ |
| ②往①试管内的溶液中滴加___________ ______________ | _____________________ | 生成物有氢氧化钠 |
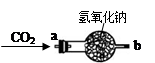
于是设计上图所示的装置继续实验探究。
| 实验操作 | 实验现象 | 实验结论 |
| ①将CO2从a口处通入装置内,再把带火星的木条放在装置b口处 | 木条复燃 | CO2在常温下能与过氧化钠反应,该反应的化学方程式为: ____________________________ |
| ②取出充分反应后的固体生成物于试管中,往试管内滴加稀盐酸,将生成的氢气通入澄清石灰水中 | 有气泡产生 石灰水变浑浊 |
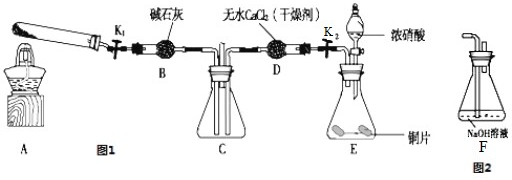
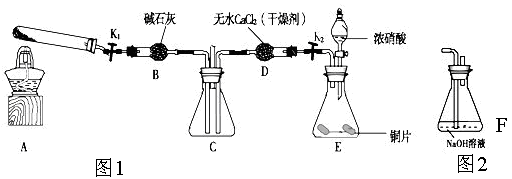
二氧化氮(NO2)是一种具有高度活性的气态物质,NO2与Na2O2均具有较强的氧化性,某研究性学习小组对二者能否发生反应进行探究。
【实验】
下列关于实验室制备NO2的说法正确的是_______
a.实验室常用铜和浓硝酸反应制取二氧化氮
b.二氧化氮常用向下排空气法收集
c.二氧化氮易溶于水,尾气可用水吸收.
d.用注射器收集的二氧化氮,压缩后颜色变浅
e.实验后容器中残留液需用碱液处理
【提出假设】
假设一:NO2与Na2O2二者不反应;
假设二:NO2能被Na2O2氧化;
假设三:
【查阅文献】
NO2在反应中能生成HNO3和HNO2;HNO2旣有氧化性,又有还原性,能被强氧化剂如KMnO4氧化。
【设计实验】
(1)实验时,将NO2气体通入盛有Na2O2的玻璃管中,淡黄色粉末完全变成白色,说明假设 不成立。
(2)若假设二成立,反应的化学方程式是 。
(3)为验证假设二是否成立,该小组同学做了如下定性实验研究,请完成下表内容。
|
实验步骤 (不要求写具体操作过程,仪器任选) |
预期的实验现象及结论 |
|
取适量的白色固体置于试管中,………… |
|
【定量分析】
若实验前该小组同学用托盘天平称量过氧化钠的质量为3.9g,充分反应后白色固体质量为8.4g,该小组同学得出假设2不成立的结论。你是否同意他们的结论,并简述理由: