题目内容
【题目】CuCl2、CuCl广泛用于有机合成的催化剂.CuCl2容易潮解; CuCl白色粉末,微溶于水,溶于浓盐酸和氨水生成络合物,不溶于乙醇. 已知:i.CuCl2+Cu+2HCl(浓)2H[CuCl2](无色) ![]() 2CuCl↓(白色)+2HCl
2CuCl↓(白色)+2HCl
ii.副反应:CuCl+H2OCuOH+2HCl; CuCl+Cl﹣═[CuCl2]﹣
(1)制取CuCl2装置如图: 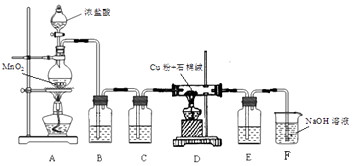
①A装置中发生反应的离子方程式是 .
②C、E 装置中盛放的是浓硫酸,作用是 .
③B中选择饱和食盐水而不用蒸馏水的原因是 .
(2)制取CuCl流程如图: 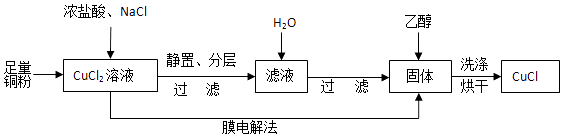
①反应①中加入NaCl的目的是;但是Cl﹣浓度过高,CuCl产率降低,原因是 .
②CuCl在潮湿的环境中易被氧化为Cu2(OH)3Cl,反应的方程式为 .
③利用膜电解法制取CuCl,阴极电极反应式为 .
④用乙醇洗涤沉淀Y的原因为 .
【答案】
(1)解:MnO2+2Cl﹣+4H+═Mn2++Cl2↑+2H2O;浓硫酸有吸水性,C、E防止CuCl2潮解;由于Cl2+H2O?H++Cl﹣+HClO;氯化钠电离出的Cl﹣ , 增大Cl﹣浓度,平衡左移,抑制了Cl2和H2O的反应,减少了Cl2消耗
(2)解:增大Cl﹣浓度,有利于生成HCuCl2;当Cl﹣浓度过高时,CuCl+Cl﹣?[CuCl2]2﹣ , 会使CuCl溶解而降低产率;4CuCl+4H2O+O2═2Cu2(OH)3Cl+2HCl;Cu2++Cl﹣+e﹣═CuCl(Cu2++e﹣═Cu+);洗去CuCl沉淀表面的杂质,减少溶解损耗;乙醇的沸点低,有利于干燥
【解析】解:(1)①A装置中为二氧化锰与浓盐酸制备氯气的反应,离子方程式为:MnO2+2Cl﹣+4H+═Mn2++Cl2↑+2H2O;所以答案是:MnO2+2Cl﹣+4H+═Mn2++Cl2↑+2H2O;②CuCl2容易潮解,故制备氯化铁的装置需保持无水环境,故C、E 装置中盛放的是浓硫酸;所以答案是:浓硫酸有吸水性,C、E防止CuCl2潮解;③制得的氯气中混有氯化氢,由于Cl2+H2OH++Cl﹣+HClO;氯化钠电离出的Cl﹣ , 增大Cl﹣浓度,平衡左移,抑制了Cl2和H2O的反应,减少了Cl2消耗,故B装置中用饱和食盐水而不用蒸馏水;所以答案是:由于Cl2+H2OH++Cl﹣+HClO;氯化钠电离出的Cl﹣ , 增大Cl﹣浓度,平衡左移,抑制了Cl2和H2O的反应,减少了Cl2消耗;(2)①反应中加入NaCl的目的是增大Cl﹣浓度,促进CuCl2+Cu+2HCl(浓)2H[CuCl2]正方向移动,有利于生成HCuCl2;当Cl﹣浓度过高时,CuCl+Cl﹣[CuCl2]2﹣ , 会使CuCl溶解而降低产率;所以答案是:增大Cl﹣浓度,有利于生成HCuCl2;当Cl﹣浓度过高时,CuCl+Cl﹣[CuCl2]2﹣ , 会使CuCl溶解而降低产率;②CuCl在潮湿的环境中易被氧化为Cu2(OH)3Cl,反应的方程式为:4CuCl+4H2O+O2═2Cu2(OH)3Cl+2HCl;所以答案是:4CuCl+4H2O+O2═2Cu2(OH)3Cl+2HCl; ③利用膜电解法制取CuCl,阴极得电子发生还原反应,则为铜离子得电子化合价升高生成CuCl,故电极反应式为:Cu2++Cl﹣+e﹣═CuCl(Cu2++e﹣═Cu+);
所以答案是:Cu2++Cl﹣+e﹣═CuCl(Cu2++e﹣═Cu+);④由题可知,CuCl微溶于水,不溶于乙醇,用乙醇洗涤沉淀可洗去CuCl沉淀表面的杂质,减少溶解损耗;乙醇的沸点低,有利于干燥;所以答案是:洗去CuCl沉淀表面的杂质,减少溶解损耗;乙醇的沸点低,有利于干燥.


