题目内容
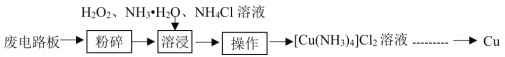
【题目】工业上可采用湿法技术从废印刷电路板中回收纯铜,其流程简图如下:
回答下列问题:
(1)开始时,将废电路板“粉碎”的目的是__________。“操作”的名称是_________________。
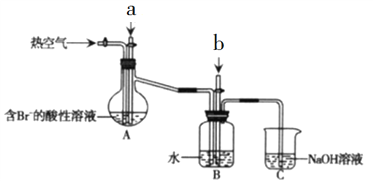
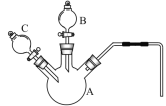
(2)某化学兴趣小组同学为探究“溶浸”过程中反应的实质,采用如图所示的装置,设计了如下对照实验。
序号 | 实验名称 | 实验步骤 | 实验现象 | |
Ⅰ | 将铜片置于H2O2溶液中 | 先向A中加入0.5g光亮的铜片,再通过B加入30%的H2O2溶液 | —————— | 开始无明显现象,10小时后,溶液变为浅蓝色,铜表面附着一层蓝色固体 |
Ⅱ | 将铜片置于硫酸酸化的H2O2溶液中 | 再通过C加入8mL 5mol/L 的稀硫酸 | 开始铜片表面产生少量气泡,随着反应的进行,气泡越来越多,溶液颜色为蓝色,铜片表面保持光亮 | |
Ⅲ | 将铜片置于有氨水的H2O2溶液中 | 再快速通过C加入8mL 5mol/L的氨水 | 立即产生大量的气泡,溶液颜色变为深蓝色,铜片表面有一层蓝色固体附着,产生的气体能使带火星的木条复燃 | |
Ⅳ | 将铜片置于加有氨水和NH4Cl的H2O2溶液中 | 先向A中加入0.5g光亮的铜片和0.2g NH4Cl固体,再通过B加入30%的H2O2溶液 | 再快速通过C加入8mL 5mol/L的氨水 | 立即产生大量的气泡,______,铜片表面依然保持光亮 |
①仪器A的名称为______________________。
②实验Ⅰ中反应的化学方程式为___________________________。
③实验Ⅱ中产生的气体是________(写化学式),实验Ⅱ比实验Ⅰ/span>现象明显的原因是__________。
④实验Ⅲ中“溶液颜色变为深蓝色”所发生反应的离子方程式为________________。
⑤实验Ⅳ中空格处实验现象为__________,加入NH4Cl的作用是______________。
【答案】增大接触面积,使反应更充分 过滤 三颈烧瓶 Cu+ H2O2=Cu(OH)2 O2 酸性条件下提高了H2O2的氧化性 Cu+H2O2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O 溶液颜色变为深蓝色 防止溶液中c(OH-)过高,生成Cu(OH)2沉淀
【解析】
本实验目的是探究“溶浸”过程中反应的实质,根据工业流程可知,铜在H2O2、NH3·H2O、NH4Cl溶液的共同作用下可以生成[Cu(NH3)4]Cl2,根据元素的化合价变化可知该过程中Cu被双氧水氧化;对比实验I和Ⅱ可知,在酸性环境下铜表面没有蓝色固体,可推测该蓝色固体应为Cu(OH)2;同时酸性环境下,Cu与双氧水的反应速率更快;根据活泼性关系可知该过程不可能产生氢气,所以产生的气体是双氧水分解生成的氧气,气泡之所以越来越多,是生成的Cu2+起到了催化作用。
(1)“粉碎”可以增大接触面积,使反应更加充分;废电路板中加入双氧水、氨气、氯化铵溶液,得到铜氨溶液和残渣,分离难溶性固体和溶液采用过滤方法,所以“操作”是过滤;
(2)①根据仪器A的结构特点可知其名称是三颈烧瓶;
②根据实验I的现象可知铜片被缓慢氧化,且生成Cu(OH)2,方程式为:Cu+ H2O2= Cu(OH)2;
③根据分析可知实验Ⅱ中产生的气体是O2;酸性条件下提高了H2O2的氧化性,所以实验Ⅱ比实验Ⅰ现象明显;
④含铜离子的溶液呈蓝色,该实验中溶液颜色变为深蓝色,结合题目所给的工艺流程可知,加入氨水后溶液中生成[Cu(NH3)4]2+,根据元素守恒和电荷守恒可得离子方程式为:Cu+H2O2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O;
⑤根据实验Ⅲ的现象可知实验Ⅳ中溶液颜色也应变为深蓝色;根据实验Ⅰ和实验Ⅱ的对比可知酸性环境下没有蓝色固体生成,氯化铵水解使溶液显酸性,所以其作用是防止溶液中c(OH-)过高,生成Cu(OH)2沉淀。