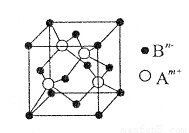
题目内容
A、B、C是在中学化学中常见的三种化合物,它们各由两种无素组成,甲、乙是两种单质。这些化合物和单质之间存在如下的关系:
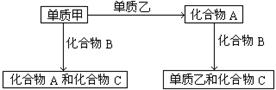
据此判断:(1)在A、B、C这三种化合物中,必定含有乙元素的是 (用A、B、C字母填写)。
(2)单质乙必定是 (填“金属”或“非金属”),其理由是 。
(3)单质乙的化学式可能是 ,则化合物B的化学式是 。
(1)A、B (2)非金属,因为A+B→乙+C,且乙为单质,可知乙元素在A、B中分别呈正、负价,所以乙是非金属。 (3)S,H2S(或N2,NH3)。
解析:
本题从物质的特殊性质突破,归纳常见物质之间的转化关系主要有:
![]() (1)直线型转化
(1)直线型转化
A B C D(酸或碱) 满足此关系的有:NH3、N2、H2S、C、Na
(2)交叉型转化
 S SO3 Na NaOH N2 NO2
S SO3 Na NaOH N2 NO2
S02 Na2O2 NO
H2S H2SO4 Na2O Na2CO3 NH3 HNO3
(3)三角型转化
 Fe Al HCl CO
Fe Al HCl CO
Fe2+ Fe3+ Al3+ AlO2_ Cl2 HClO C CO2
(4)特殊反应:
①高温进行的主要反应:2Al+Fe2O3![]() 2Fe+Al2O3 ;3Fe+4H2O(g)
2Fe+Al2O3 ;3Fe+4H2O(g)![]() Fe3O4+4H2;C+H2O
Fe3O4+4H2;C+H2O![]() CO+H2 ; C+SiO2
CO+H2 ; C+SiO2![]() 2CO+Si等
2CO+Si等
②有催化剂参与的反应主要有:4NH3+5O2 ![]() 4NO+6H2O ;2KClO3
4NO+6H2O ;2KClO3![]() 2KCl+3O2;2SO2+O2
2KCl+3O2;2SO2+O2![]() 2SO3 N2+3H2
2SO3 N2+3H2![]() 2NH3
2NH3

 键和
键和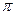 键的数目之比为 ;F、G对应的氢化物中键能大小为F—H键 G—H键。
键的数目之比为 ;F、G对应的氢化物中键能大小为F—H键 G—H键。