题目内容
将12.4g碱石灰制成溶液,加入13.7g Na2CO3和NaHCO3,反应后得沉淀15g,经测定,反应后溶液中不含Ca2+、CO32+、HCO3-。求
(1) CaO和NaOH各多少g? (2)Na2CO3和NaHCO3各多少g?
(1) CaO和NaOH各多少g? (2)Na2CO3和NaHCO3各多少g?
(1) CaO8.4g ,NaOH 0.15mol(2)Na2CO3 5.3g ,NaHCO38.4g
运用守恒法解题既可避免书写繁琐的化学方程式,提高解题的速度,又可避免在纷纭复杂的解题背景中寻找关系式,提高解题的准确度。
据题意CaO和Na2CO3、NaHCO3均全部转化为CaCO3沉淀,据Ca原子和C原子两种原子的守恒关系,便可列出关系式:
nCaO=nCa(OH)2=nCaCO3=nNa2CO3+nNaHCO3
可得关系式:
CaO ~ CaCO3 ~ (Na2CO3+NaHCO3)
56g 100g 1mol
x 15g y
解得 x="8.4g" y=0.15mol
所以mNaOH=12.4g-8.4g=4g
设Na2CO3物质的量为a,则NaHCO3物质的量为0.15mol-a
106g/mol a+84g/mol×(0.15mol-a)=13.7g
解得a=0.05mol
所以mNa2CO3=0.05mol×106g/mol="5.3g" mNaHCO3=13.7g-5.3g=8.4g。
据题意CaO和Na2CO3、NaHCO3均全部转化为CaCO3沉淀,据Ca原子和C原子两种原子的守恒关系,便可列出关系式:
nCaO=nCa(OH)2=nCaCO3=nNa2CO3+nNaHCO3
可得关系式:
CaO ~ CaCO3 ~ (Na2CO3+NaHCO3)
56g 100g 1mol
x 15g y
解得 x="8.4g" y=0.15mol
所以mNaOH=12.4g-8.4g=4g
设Na2CO3物质的量为a,则NaHCO3物质的量为0.15mol-a
106g/mol a+84g/mol×(0.15mol-a)=13.7g
解得a=0.05mol
所以mNa2CO3=0.05mol×106g/mol="5.3g" mNaHCO3=13.7g-5.3g=8.4g。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
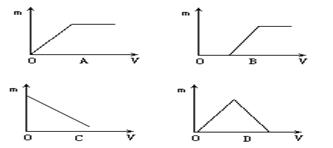
 气体后,溶液变浑浊的是 ( )
气体后,溶液变浑浊的是 ( )