题目内容
可以肯定溶液中大量存在CO32-的理由是 ( )
| A.加入AgNO3溶液,有大量白色沉淀产生 | B.加入酸,有无色无味气体产生 |
C.加入BaCl2溶液时有白色沉淀产生,再加稀盐酸沉淀溶解,产生可使澄清石灰水变浑浊的无色无味的气体        | |
| D.加入Ba(OH)2溶液有白色沉淀产生,再加稀盐酸如C所述 |
C
溶液中含有Cl-、SO32-时,可与AgNO3溶液反应产生白色沉淀,A不正确。HCO3-与酸反应会产生无色无味CO2气体,B不正确。向含有HCO3-的溶液中加入
Ba(OH)2时:HCO3-+OH-+Ba2+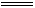 BaCO3↓+H2O,再加盐酸BaCO3+2H+
BaCO3↓+H2O,再加盐酸BaCO3+2H+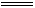 Ba2++CO2↑
Ba2++CO2↑
+H2O,其现象与CO32-反应现象相同,D选项不正确。
Ba(OH)2时:HCO3-+OH-+Ba2+
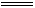 BaCO3↓+H2O,再加盐酸BaCO3+2H+
BaCO3↓+H2O,再加盐酸BaCO3+2H+ Ba2++CO2↑
Ba2++CO2↑+H2O,其现象与CO32-反应现象相同,D选项不正确。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目