题目内容
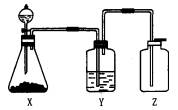
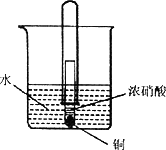
下列三个问题均与下图中实验装置有关,请选择A—D序号填入空格中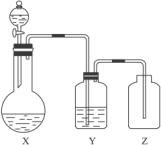
(1)制取某无色非金属氧化物气体时,烧瓶X内的药品应是
A.铜与稀HNO3
B.铜与浓HNO3
C.CaCO3与稀H2SO4
D.Na2SO3与浓盐酸
(2)洗气瓶Y中所装液体应是(不允许非水杂质混在气体中)
A.浓H2SO4
B.NaOH溶液
C.饱和NaHSO3溶液
D.NaHCO3溶液
(3)检验集气瓶口是否集满气体,置于瓶口的滤纸应沾上的溶液是
A.BaCl2溶液
B.KMnO4酸性溶液
C.KI淀粉
D.石灰水
(1)D(2)C(3)B
解析:(1)铜与稀HNO3反应需加热,且得到无色NO气体易被空气中O2氧化为红棕色NO2。铜与浓HNO3反应直接生成NO2,均不符合题意。CaCO3与稀H2SO4反应生成CaSO4覆盖在CaCO3表面,反应逐渐停止,不能制得CO2。Na2SO3与浓盐酸常温下反应生成无色气体,符合题意。
(2)从X中出来的SO2中将混有较多的HCl和少量的水蒸气,应选用饱和NaHSO3除掉HCl,而SO2不与NaHSO3反应,能实现除去气体中非水杂质的目的。
(3)SO2与BaCl2、KI不反应;SO2与石灰水反应生成CaSO3沉淀,在滤纸上不易观察,也不能作为检验手段;SO2遇强![]() 可被氧化,可使KMnO4酸性溶液褪色,现象明显,易于观察,符合题意。
可被氧化,可使KMnO4酸性溶液褪色,现象明显,易于观察,符合题意。

练习册系列答案
相关题目
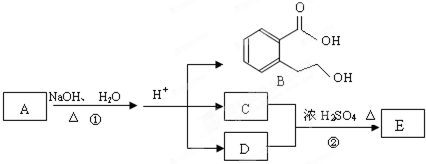

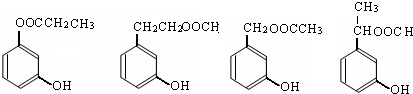 任意1种
任意1种