题目内容
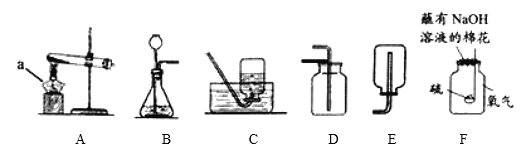
【题目】用如图所示实验装置进行物质性质的探究实验。下列说法正确的是

A. ②中溴水褪色,说明SO2具有漂白性
B. ③中溶液由黄色变浅绿色,溶液的pH变小
C. ④中出现白色浑浊,说明亚硫酸的酸性比硅酸弱
D. ⑤中出现深红色沉淀(Cu2S03CuSO32H2O),发生的反应中氧化剂与还原剂的物质的量之比为3:2
【答案】B
【解析】A. ②中溴水褪色,二氧化硫将溴还原生成氢溴酸,同时生成硫酸,说明SO2具有还原性,选项A错误;B. ③中溶液由黄色变浅绿色,二氧化硫、氯化铁和水反应生成氯化亚铁、硫酸和盐酸,溶液的pH变小,选项B正确;C、④中出现白色浑浊,说明亚硫酸的酸性比硅酸强,选项C错误;D、⑤中出现深红色沉淀(Cu2S03CuSO32H2O),发生的反应中氧化剂与还原剂的物质的量之比为2: 3,选项D错误。答案选B。

 阅读快车系列答案
阅读快车系列答案【题目】工业以黄铜矿(主要成分是CuFeS2)为原料制备粗铜,进一步以粗铜为原料制备CuSO4·5H2O晶体。工艺流程如下(部分操作和条件略):
I. 煅烧黄铜矿,得到粗铜(含铁及铁、铜的化合物等);
II. 向粗铜中加入稀H2SO4和稀HNO3,并使产生的NO与H2O、O2反应;
III. 调节Ⅱ中所得溶液的pH,过滤;
Ⅳ. 将Ⅲ中滤液浓缩后冷却结晶,过滤,得到CuSO4·5H2O晶体。
已知:生成氢氧化物的pH
Cu(OH)2 | Fe(OH)3 | |
开始沉淀时 | 4.8 | 1.5 |
完全沉淀时 | 6.7 | 2.8 |
注:金属离子的起始浓度为0.1 mol/L
请回答:
(1)I中主要发生如下两个化学反应。请将反应ii的化学方程式补充完整。
i. 2CuFeS2+4O2![]() Cu2S+3SO2+2FeO
Cu2S+3SO2+2FeO
ii. ![]() Cu2S+
Cu2S+![]() O2
O2 ![]()
![]() _________+
_________+ ![]() SO2
SO2
(2)II中NO与H2O、O2反应的化学方程式是_________。
(3)III中的滤渣主要是Fe(OH)3。调节溶液的pH时,pH范围是_________。
(4)有关上述过程的说法中,正确的是_________(填序号)。
a. I中尾气含有SO2,可综合利用制备H2SO4。
b. II中稀HNO3的作用之一是使Cu单质转化为Cu2+
c. 在上述过程中,HNO3可循环利用