题目内容
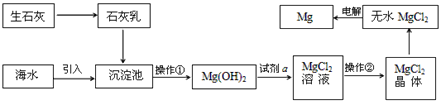
【题目】目前世界上60%的镁是从海水提取的。海水提镁的主要流程如下:
提示:①MgCl2晶体的化学式为MgCl26H2O;②MgO的熔点为2852℃,无水MgCl2的熔点为714℃。
(1)操作①的名称是 ________,操作②的名称___________、冷却结晶、过滤。
(2)试剂a的名称是_____________,涉及的相关化学方程式为__________;
(3)用氯化镁电解生产金属镁的化学方程式为:_____________________________。
【答案】过滤 蒸发浓缩 盐酸 Mg(OH)2+2HCl=2MgCl2+2H2O MgCl2(熔融) ![]() Mg+Cl2↑
Mg+Cl2↑
【解析】
海水中的Mg2+和石灰乳中的OH-生成Mg(OH)2沉淀,过滤后,加盐酸溶解得到MgCl2溶液,再蒸发溶液使其浓度变大,然后冷却使晶体析出,过滤得到MgCl2·6H2O。得到的MgCl2·6H2O再在HCl的气流中加热得到无水MgCl2,最后电解熔融的MgCl2得到金属镁。
(1)在沉淀池中石灰乳和海水中的镁离子生成氢氧化镁沉淀。经过滤得到氢氧化镁固体,所以操作①的名称是过滤。从氯化镁溶液中获得氯化镁晶体,需要经过蒸发浓缩,冷却结晶,过滤等操作,所以操作②的名称是蒸发浓缩。故答案为:过滤,蒸发浓缩;
(2)氢氧化镁转变成氯化镁溶液,需要加盐酸,所以试剂a名称是盐酸。发生的反应是:Mg(OH)2+2HCl=2MgCl2+2H2O,故答案为:盐酸,Mg(OH)2+2HCl=2MgCl2+2H2O;
(3)用氯化镁生产金属镁需要电解熔融的氯化镁,方程式为:MgCl2(熔融)![]() Mg+Cl2↑。
Mg+Cl2↑。

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目