题目内容
A 、B、C、D、E、F、G是元素周期表中1~36号的七种常见元素,其原子序数依次增大。其中B、D、G三种元素的原子核外未成对电子数均等于其周期序数;F的单质常用于工业上制漂白粉;D与A、E均可形成原子个数比为1:1和1:2的化合物。
、B、C、D、E、F、G是元素周期表中1~36号的七种常见元素,其原子序数依次增大。其中B、D、G三种元素的原子核外未成对电子数均等于其周期序数;F的单质常用于工业上制漂白粉;D与A、E均可形成原子个数比为1:1和1:2的化合物。
请回答下列问题:
⑴F在元素周期表中的位置_____ ________,B、C、D、E元素第一电离能由大到小的顺序是____________(用元素符号表示);
________,B、C、D、E元素第一电离能由大到小的顺序是____________(用元素符号表示);
⑵F、G两元素的单质间反应所得产物为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醇,丙酮等有机溶剂。据此判断该产物晶体为______晶体;该产物中G元素相应价态离子的核外电子排布式为__________________;
⑶B、C、D均可与A形成10电子和18电子的分子。
①在B、C、D分别与A形成的10电子分子中,极性最强的共价键是______ (用化学键表示)。A、B、C 三元素形成的最简单分子中
三元素形成的最简单分子中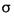 键与
键与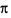 键个数比为______;
键个数比为______;
②C、D分别与A形成的18电子分子X、Y可用作火箭推进剂。已知16g液态X与足量液态Y充分反应生成一种液态化合物和一种气态单质,并放出838kJ的热量,试写出X与Y反应的热化学方程式________________________。
 、B、C、D、E、F、G是元素周期表中1~36号的七种常见元素,其原子序数依次增大。其中B、D、G三种元素的原子核外未成对电子数均等于其周期序数;F的单质常用于工业上制漂白粉;D与A、E均可形成原子个数比为1:1和1:2的化合物。
、B、C、D、E、F、G是元素周期表中1~36号的七种常见元素,其原子序数依次增大。其中B、D、G三种元素的原子核外未成对电子数均等于其周期序数;F的单质常用于工业上制漂白粉;D与A、E均可形成原子个数比为1:1和1:2的化合物。请回答下列问题:
⑴F在元素周期表中的位置_____
 ________,B、C、D、E元素第一电离能由大到小的顺序是____________(用元素符号表示);
________,B、C、D、E元素第一电离能由大到小的顺序是____________(用元素符号表示);⑵F、G两元素的单质间反应所得产物为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醇,丙酮等有机溶剂。据此判断该产物晶体为______晶体;该产物中G元素相应价态离子的核外电子排布式为__________________;
⑶B、C、D均可与A形成10电子和18电子的分子。
①在B、C、D分别与A形成的10电子分子中,极性最强的共价键是______ (用化学键表示)。A、B、C
 三元素形成的最简单分子中
三元素形成的最简单分子中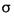 键与
键与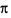 键个数比为______;
键个数比为______;②C、D分别与A形成的18电子分子X、Y可用作火箭推进剂。已知16g液态X与足量液态Y充分反应生成一种液态化合物和一种气态单质,并放出838kJ的热量,试写出X与Y反应的热化学方程式________________________。
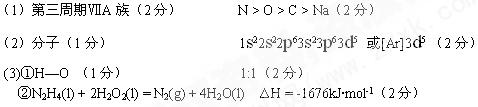
略

练习册系列答案
相关题目
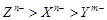
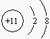 ,元素Y的原子结构示意图为
,元素Y的原子结构示意图为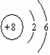 ,则元素X与元素Y形成的化合物的化学式为( )
,则元素X与元素Y形成的化合物的化学式为( )
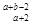 R
R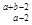 R
R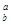 R
R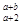 R
R 1列,稀有气体为18列。按这个规定,下列说法错误的是
1列,稀有气体为18列。按这个规定,下列说法错误的是