题目内容
【题目】海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在。某课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(以让碘化物充分溶解在水中),得到 海带灰悬浊液,再按以下实验流程提取单质碘:
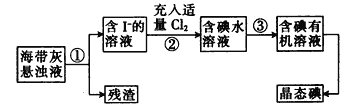
(1)实验操作①的名称:__________。
(2)用于灼烧海带的实验仪器是_________。(选填字母)
A.烧杯 B.蒸发皿 C.试管 D.坩埚
(3)操作③中所用的有机溶剂可以是__________。(选填字母)
A.苯(沸点80℃) B.四氯化碳(沸点76.8℃)
C.酒精(沸点 78℃) D.裂化汽油(易与碘反应)
(4)操作过程③可以分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50mL碘水和15mL有机溶剂(你所选的)加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层。
上述操作的正确顺序是:____________(用字母表示)
(5)从含碘的有机溶液中提取碘和回收有机溶剂,还需要经过蒸馏,如图是利用水浴加热的方式进行 蒸馏的实验装置,其中错误的有_________处。(碘的沸点184.3℃)

(6)该实验进行蒸馏时,使用水浴加热的优点是________,最后晶态碘在________里聚集。
【答案】过滤 D AB CBDAHGEF 3 受热均匀且容易控制温度 蒸馏烧瓶
【解析】
以海带为原料获得少量碘单质:将海带在坩埚中灼烧得到海带灰,将海带灰浸泡得到海带灰悬浊液,然后采用过滤的方法将残渣和溶液分离,得到含有碘离子的溶液,向水溶液中通入足量Cl2,发生的反应为2I-+Cl2=2Cl-+I2,向含有碘单质的溶液中加入萃取剂萃取,分液得到含碘有机溶液,最后蒸馏得到碘单质,据此分析解答。
(1)根据流程图,经过实验操作①,海带灰悬浊液分离为溶液和残渣,因此实验操作①为过滤,故答案为:过滤;
(2)灼烧海带时用坩埚盛放海带,用带铁圈的铁架台或三脚架和泥三角上放置坩埚,用酒精灯进行加热,所以灼烧海带时需要用到的实验仪器是坩埚、带铁圈的铁架台或三脚架、泥三角、酒精灯,故选D;
(3)操作③是将含碘水溶液变成含碘有机溶液,为萃取,所用的有机溶剂可以是苯或四氯化碳,酒精易溶于水,不能选用,裂化汽油易与碘反应,也不能选用,故答案为:AB;
(4)萃取的实验步骤为:C.检验分液漏斗活塞和上口的玻璃塞是否漏液;B.把50mL碘水和15mL有机溶剂(你所选的)加入分液漏斗中,并盖好玻璃塞;D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;A.把盛有溶液的分液漏斗放在铁架台的铁圈中;H.静置、分层;G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;E.旋开活塞,用烧杯接收溶液;F.从分液漏斗上口倒出上层液体,故答案为:CBDAHGEF;
(5)由图可知,加热烧杯未垫上石棉网;蒸馏时温度计插入溶液,应是水银球应与烧瓶支管口相平;冷却水应下进上出。则错误为没有用石棉网,温度计的水银球插入溶液中,冷却水方向接反了,故答案为:3;
(6)该实验进行蒸馏时,使用水浴的优点是:受热均匀且容易控制温度;四氯化碳沸点低于碘单质沸点,所以最后晶态碘在蒸馏烧瓶里聚集,故答案为:受热均匀且容易控制温度;蒸馏烧瓶。

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10﹣5molL﹣1 | K1=4.4×10﹣7molL﹣1 K2=5.6×10﹣11molL﹣1 | 3.0×10﹣8molL﹣1 |
请回答下列问题:
(1)同浓度的CH3COO﹣、HCO3﹣、CO32﹣、ClO﹣结合H+的能力由强到弱的顺序为________。
(2)常温下0.1molL﹣1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是________(填字母序号,下同)。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)c(OH﹣) D.c(OH-)/ c(H+) E.c(H+)c(CH3COO-)/ c(CH3COOH)
若该溶液升高温度,上述5种表达式的数据增大的是________。
(3)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:
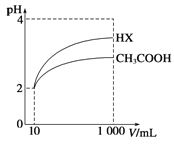
则HX的电离平衡常数________(填“大于”、“等于”或“小于”)醋酸的平衡常数.稀释后,HX溶液中由水电离出来的c(H+)________(填“大于”、“等于”或“小于”)醋酸的溶液中由水电离出来的c(H+),理由是____________________。
(4)已知100℃时,水的离子积为1×10﹣12, 该温度下测得某溶液pH=7,该溶液显________(填“酸”、“碱”或“中”)性.将此温度下pH=1的H2SO4溶液aL与pH=11的NaOH溶液bL混合,若所得混合液pH=2,则a∶b=________。