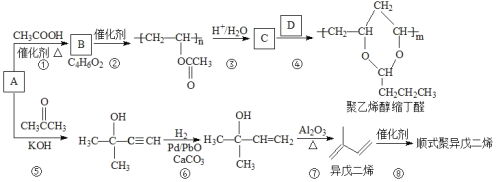
��Ŀ����
����Ŀ���ߴ��ȵ������ǵ��͵����ǽ������ϣ��ֳ����뵼�������ϣ����ķ��ֺ�ʹ��������������һ���������������ֲ��Ͽ������з����Ʊ���
SiO2![]() Si(��)
Si(��)![]() SiHCl3
SiHCl3![]() Si(��)������˵����ȷ����(����)
Si(��)������˵����ȷ����(����)
A.����ٵĻ�ѧ����ʽΪSiO2��C![]() Si��CO2��
Si��CO2��
B.����١��ڡ�����ÿ���ɻ�Ӧ1 mol Si��ת��4 mol����
C.����������������ᷴӦ�����費��������ᷴӦ
D.SiHCl3(�е�33.0 ��)�к���������SiCl4(�е�67.6 ��)��ͨ������(�����)���ᴿSiHCl3
���𰸡�D
��������
A.���������������C��Ӧ����CO���壻
B.������ԭ��Ӧ��ʧ�����غ��жϼ��ɣ�
C.����������ᷴӦ����SiF4��������
D.�ɷе����֪��,Ϊ���30�����ϵ�����Һ�塣
A.���������������C��Ӧ����CO����,������ٵĻ�ѧ����ʽΪ: SiO2��2C![]() Si��2CO������A����
Si��2CO������A����
B.�������Si�Ļ��ϼ۽���4��ת�Ƶ�����Ϊ4mol�������������SiHCl3����Ԫ�ػ��ϼ�����2��������й�Ԫ�صĻ��ϼ۽���2������ÿ���ɻ�Ӧ1molSi����ת��2mol����,��B����
C.����������ᷴӦ����SiF4������,��C����
D.�е����30�����ϵ�����Һ����Բ�������ķ������룬��D��ȷ��
�ʴ�ѡD��

 �����ܿ����ϵ�д�
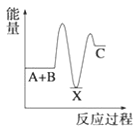
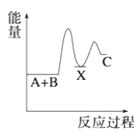
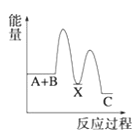
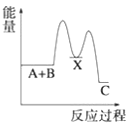
�����ܿ����ϵ�д�����Ŀ���ס��ҡ��������������������У��ס��ҡ����о�����ij����ͬ��Ԫ�أ�����֮�������ͼ��ʾת����ϵ(��Ӧ���������ֲ�������ȥ)�������й����ʵ��ƶϲ���ȷ����(����)

ѡ�� | ���� | ���� |
A | ��ΪAl(OH)3 | ������������ |
B | ��ΪNa2CO3��Һ | �������CO2 |
C | ��ΪFe | ������������ |
D | ��ΪN2 | ����������� |
A. A B. B C. C D. D