��Ŀ����
����ʱ������������ȷ����
| A��pH=9��NH4Cl��NH3��H2O�����Һ��c(Cl-)>c(NH4+) |
| B��pH=2.5�Ŀ�����c��H+����pH=3.5������ˮ��c��H+����1 0�� |
| C��AgCl��0.1 mol��L CaCl2��Һ��0.l mol��L NaCl��Һ�е��ܽ����ͬ |
| D��1 mL l mol l L Na2CO3��Һ��ˮϡ����100 mL��pH��Kw����С |
B
�������������A��pH=9��NH4Cl��NH3��H2O�����Һ��NH3��H2O�ĵ���̶ȴ���NH4Cl��ˮ��̶ȣ�����c(Cl-)<c(NH4+)������B��pH=2.5�Ŀ�����c��H+��=1��10-2.5mol/L��pH=3.5������ˮ��c��H+��=1��10-3.5mol/L��ǰ���Ǻ��ߵ�10������ȷ��C��0.1 mol��L CaCl2��Һ��0.l mol��L NaCl��Һ�е������ӵ�Ũ�Ȳ�ͬ������AgCl���ܽ�Ȳ�ͬ������D��Kw���¶ȳ������¶Ȳ��䣬Kw���䣬����ѡB��
���㣺������Һ������Ũ�ȵıȽϣ�pH�ļ��㣬��Һϡ������pH��Kw���жϣ�ͬһ�����ڲ�ͬ�ܼ��е��ܽ�ȵ��ж�

 ��У����ϵ�д�
��У����ϵ�д������£������й����ʵ���Ũ�ȹ�ϵ��ȷ���ǣ� ��
| A�������ʵ���Ũ�ȵ���Һ�У�ˮ�������c��H+����HCl��CH3COOH |
| B��pH��ͬ����Һ�У�c��Na2CO3����c��NaHCO3�� |
| C����Na2SO3��Һ�У�c��Na+��= 2c��SO32-��+ c��HSO3-��+ c��OH-�� |
| D��0.1mol��L-1NaHS��Һ�У�c��Na+��= c��HS���� |
��֪ˮ��25���95��ʱ�������ƽ��������ͼ��ʾ������˵�������
| A��A���ߴ���25��ʱˮ�ĵ���ƽ������ |
| B����95��ʱ��pH=6����Һ������ |
| C��25��ʱ����10mLpH=12��NaOH��Һ��1mLpH=1��H2SO4 ��Һ��ϣ�������Һ��pH=7 |
| D��95��ʱ������������ʵ���Ũ�ȵ�HA��Һ��NaOH��Һ��Ϻ������Һ��pH=6ʱ��˵��HA��Ϊ���� |
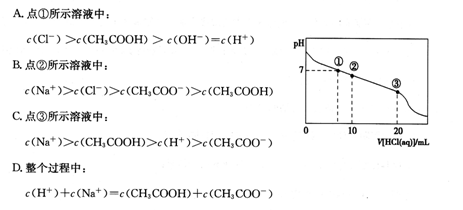
�����£���20.00 mL 0.100 mol��L��1 CH3COONa��Һ����μ���0.100 0 mol��L��1���ᣬ��Һ��pH��������������Ĺ�ϵ����ͼ��ʾ(�����ǻӷ�)������˵����ȷ����
| A�������ʾ��Һ�У�c(CH3COOH)��c(Cl��)��c(OH��)��c(H��) |
| B�������ʾ��Һ�У�c(Na��)��c(Cl��)��c(CH3COO��)��c(CH3COOH) |
| C�������ʾ��Һ�У�c(CH3COOH)��c(Na��)��c(H��)��c(CH3COO��) |
| D�����������п��ܳ��֣�c(H��)��c(Na��)��c(CH3COOH)��c(CH3COO��) |
�����£����и���������ָ����Һ��һ���ܴ����������
A�������̪��Һ�Ժ�ɫ����Һ�У�K����Na����Cu2����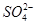 |
B���������NaOH��Һ������ϡH2SO4ʱ�����ܲ�����ɫ��������Һ��Al3����Ba2����Cl����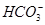 |
C��ˮ���������c(H��)��10��13mol��L��1����Һ�У�Na����Cl���� �� ��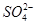 |
D��0.1 mol��L��1HNO3��Һ�У�Mg2����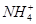 ��Fe2����Cl�� ��Fe2����Cl�� |
�����£�Ũ�Ⱦ�Ϊ0.1 mol/L ��������������Һ����pH�ⶨ���±���ʾ��
| ��� | �� | �� | �� | �� |
| ��Һ | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
| pH | 8.8 | 9.7 | 11.6 | 10.3 |
A��������Һ�У�ˮ�ĵ���̶Ȣ٣��ڣ��ܣ���
B��Na2CO3��NaHCO3��Һ�У�����������ͬ
C������Ũ�ȵ�CH3COOH��HClO��Һ�Ƚϣ�pHС����HClO
D��Na2CO3��Һ�У� c(Na��) �� c(CO32��)��c(HCO3��)��c(H2CO3)
��ͼ��ʾ��Һ��c(H��)��c(OH��)�Ĺ�ϵ�������жϴ������
| A������������������c(H��)��c(OH��)��Kw |
| B��M��������������c(H��)��c(OH��) |
| C��ͼ��T1��T2 |
| D��XZ������������pH��7 |