题目内容
【题目】近两年来无人驾驶汽车的大热使得激光雷达成为人们关注的焦点,激光雷达的核心部件需要一种氮化铝(A1N)导热陶瓷片。下图是从铝土矿(主要成分为A12O3,还含有少量SiO2、 Fe2O3等杂质)中提取A12O3并生产A1N的工艺流程:
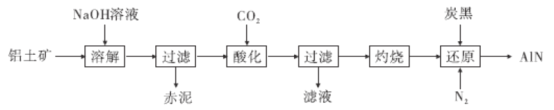
(1)“溶解”时,已知溶液中的硅酸钠与偏铝酸钠可发生反应:2Na2SiO3+2NaA1O2+2H2O=== Na2Al2Si2O8↓ +4NaOH。赤泥的主要成分除了生成的Na2Al2Si2O8还有________(写出化学式),Na2Al2Si2O8用氧化物的形式表示为______________________________________________________。
(2) “酸化”时通入过量CO2与NaA1O2反应生成NaHCO3 和另一种白色沉淀,试写出该反应的化学方程式________________________________;实验室过滤需用到的玻璃仪器有烧杯、_____________________、玻璃棒。
(3)“还原”时,炭黑在高温下被氧化为CO,反应的化学方程式为_____________;
(4)已知:AlN+NaOH + H2O===NaA1O2+NH3 ↑。现取氮化铝样品5.0 g(假设杂质只含有炭黑)加到100 mL 1. 0 mol L-1的NaOH溶液中恰好反应完,则该样品中A1N的质量分数为 ___________________。
【答案】Fe2O3 Na2OAl2O32SiO2 NaAlO2+CO2+2H2O===Al(OH)3↓+NaHCO3 漏斗 Al2O3+N2+3C![]() 2AlN+3CO ↑ 82%
2AlN+3CO ↑ 82%
【解析】
铝土矿(主要成分为A12O3,还含有少量SiO2、 Fe2O3等杂质),铝土矿中加入氢氧化钠溶液,SiO2和A12O3溶于氢氧化钠溶液,溶液中的硅酸钠与偏铝酸钠发生反应:2Na2SiO3+2NaA1O2+2H2O=== Na2Al2Si2O8↓ +4NaOH,氧化铁不溶于氢氧化钠溶液,所以过滤得到的赤泥为Fe2O3、Na2Al2Si2O8,滤液主要为偏铝酸钠溶液,偏铝酸钠溶液中通入过量的二氧化碳酸化得到的沉淀为氢氧化铝,过滤得到的滤液主要为NaHCO3溶液,氢氧化铝灼烧得到氧化铝,氧化铝、碳黑、氮气在高温下生成氮化铝,同时碳被氧化为CO,据此解答此题。
(1)氧化铁与氢氧化钠不反应,则赤泥的主要成分为Fe2O3、Na2Al2Si2O8,Na2Al2Si2O8用氧化物的形式表示为Na2OAl2O32SiO2;
答案为:Fe2O3 ;Na2OAl2O32SiO2 ;
(2)“酸化”时通入过量CO2与NaA1O2反应生成Al(OH)3,反应的化学方程式为:NaAlO2+CO2+2H2O===Al(OH)3↓+NaHCO3;实验室过滤需用到的玻璃仪器有烧杯、漏斗、玻璃棒;
答案为:NaAlO2+CO2+2H2O===Al(OH)3↓+NaHCO3;漏斗;
(3)氧化铝、碳黑、氮气在高温下生成氮化铝,同时碳黑被氧化为CO,反应的化学方程式为:Al2O3+N2+3C![]() 2AlN+3CO ↑;
2AlN+3CO ↑;
答案为:Al2O3+N2+3C![]() 2AlN+3CO ↑;漏斗;
2AlN+3CO ↑;漏斗;
(4)加到100 mL 1. 0 mol L-1的NaOH溶液中恰好反应完,则n(NaOH)=0.1L1.0mol/L=0.1mol,根据反应AlN+NaOH + H2O===NaA1O2+NH3 ↑可知,n(AlN)= n(NaOH)=0.1mol,所以AlN的质量分数为:![]() ;
;
答案为:82%;

 阅读快车系列答案
阅读快车系列答案【题目】动手实践:某同学探究同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验步骤”与“实验现象”前后不一定是对应关系)。
实验步骤 | 实验现象 |
①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色 |
②向新制的Na2S溶液中滴入新制氯水 | B.有气体产生,溶液变成浅红色 |
③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体 |
⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
⑥向AlCl3溶液中滴加溶液至过量 | F.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究___元素性质递变规律。
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞溶液等。
仪器:①___,②___,③___,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式)___
实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
实验现象(填A~F) |
①的化学方程式___,
②的化学方程式___。
(4)实验结论:
失电子能力:___,得电子能力:___。
【题目】在恒温、恒容条件下发生下列反应:2X2O5 (g) ![]() 4XO2(g) +O2(g) △H>0,T温度下的部分实验数据为:
4XO2(g) +O2(g) △H>0,T温度下的部分实验数据为:
t/s | 0 | 50 | 100 | 150 |
c(X2O5) mol/L | 4.00 | 2.50 | 2.00 | 2.00 |
下列说法错误的是
A. T温度下的平衡数为K=64 (mol/L)3,100s时转化率为50%
B. 50s 内 X2O5分解速率为 0.03 mol/ (Ls)
C. T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则Kl>K2
D. 若只将恒容改为恒压,其它条件都不变,则平衡时X2O5的转化率和平衡常数都不变
【题目】利用实验器材(规格和数量不限,省略夹持装置),能够完成相应实验的有几项( )
实验器材 | 相应实验 | |
① | 量筒、温度计、烧杯、碎纸条、盖板 | 中和热的测定 |
② | 烧杯、分液漏斗 | 用饱和Na2CO3溶液除去乙酸乙酯中的乙酸和乙醇 |
③ | 量筒、玻璃捧、烧杯、100mL容量瓶 | 用浓盐酸配制100mL0.1molL-1的稀盐酸溶液 |
④ | 烧杯、酸式滴定管、碱式滴定管、锥形瓶 | 用H2SO4标准液滴定未知浓度的NaOH溶液 |
⑤ | 蒸馏烧瓶、酒精灯、温度计、直形冷凝管、锥形瓶、牛角管、石棉网 | 分离甲醇和甘油的混合物 |
⑥ | 坩埚、酒精灯、玻璃棒、泥三角、三脚架 | 从食盐水中得到NaCl晶体 |
A.2项B.3项C.4项D.5项