��Ŀ����
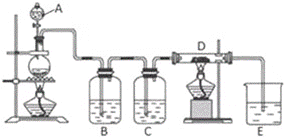
����Ŀ����ͼ��ʾ��������A�е�Ũ����μӵ�ʢ��MnO2����ƿ�У����Ⱥ��������������ͨ��װ��B��C��Ȼ����ͨ�����ȵ�ʯӢ������D�����������ۣ�����ش�
��1������A��������____����ƿ�з�Ӧ�Ļ�ѧ����ʽ��____�������������___������ţ�
�������� �ڻ�ԭ�� ������
��2��װ��B��ʢ��Һ����___������ͨ��װ��B��Ŀ����___��װ��C��ʢ�ŵ�Һ����___��
��3��D�з�Ӧ�Ļ�ѧ����ʽ��____��
��4���ձ�E��ʢ�ŵ�Һ����___��������___����Ӧ�����ӷ���ʽ��___��
��5�����ϱ���D�в������������ʣ�����������������ȴ��������������H2O��g�����ҷ�Ӧ��Ϊ�ռ�D�в����D��E֮�䣬�������ռ�װ���⣬����Ҫ����___װ�á�
���𰸡���Һ©�� MnO2+4HCl��Ũ��![]() MnCl2+Cl2��+2H2O �ڢ� ����NaCl��Һ ���������л��е�����HCl Ũ���� 2Fe+3Cl2
MnCl2+Cl2��+2H2O �ڢ� ����NaCl��Һ ���������л��е�����HCl Ũ���� 2Fe+3Cl2![]() 2FeCl3 ����������Һ β����������ֹ������Ⱦ���� Cl2+2OH��=Cl��+ClO��+H2 ����
2FeCl3 ����������Һ β����������ֹ������Ⱦ���� Cl2+2OH��=Cl��+ClO��+H2 ����
��������
װ������ƿ��Ϊ�������̣�����AΪ��Һ©������Ũ���������������ڼ��ȵ������¼��ȷ�Ӧ������������ӦΪ��MnO2+4HCl��Ũ��![]() MnCl2+Cl2��+2H2O�����ɵ������к������Ȼ����ˮ������ͨ��װ��B�еı���ʳ��ˮ��ȥ�Ȼ��⣬ͨ��װ��C�е�Ũ�����ȥˮ�������������������װ��D�������ȷ�Ӧ�����Ȼ�����2Fe+3Cl2
MnCl2+Cl2��+2H2O�����ɵ������к������Ȼ����ˮ������ͨ��װ��B�еı���ʳ��ˮ��ȥ�Ȼ��⣬ͨ��װ��C�е�Ũ�����ȥˮ�������������������װ��D�������ȷ�Ӧ�����Ȼ�����2Fe+3Cl2![]() 2FeCl3��ʣ������ͨ������������Һ���գ��ݴ˷ֽ���
2FeCl3��ʣ������ͨ������������Һ���գ��ݴ˷ֽ���
(1)�����������֪AΪ��Һ©������ƿ��Ũ������������̼������������ķ�Ӧ����ѧ����ʽΪ��MnO2+4HCl��Ũ��![]() MnCl2+Cl2��+2H2O�����ݲ����֪���˷�Ӧ��Ũ���������Ժͻ�ԭ�Ե����ã��ڢ۷������⣻
MnCl2+Cl2��+2H2O�����ݲ����֪���˷�Ӧ��Ũ���������Ժͻ�ԭ�Ե����ã��ڢ۷������⣻
�ʴ�Ϊ����Һ©���� MnO2+4HCl��Ũ��![]() MnCl2+Cl2��+2H2O���ڢۣ�
MnCl2+Cl2��+2H2O���ڢۣ�
(2)��Ӧ���ɵ������к����Ȼ����ˮ�����������壬�Ȼ��⼫������ˮ�������ڱ���ʳ��ˮ���ܽ��Լ�����ͨ������ʳ��ˮ��ȥ�Ȼ������壬ͨ��Ũ������Һ����ˮ������װ��B��ʢ��Һ���DZ���ʳ��ˮ������ͨ��װ��B��Ŀ�������������л��е�����HCl��װ��C��ʢ�ŵ�Һ����Ũ���ᣬ����ͨ��װ��C��Ŀ��������ˮ����������������
�ʴ�Ϊ������ʳ��ˮ�����������л��е�����HCl��Ũ���
(3)���������ͨ��װ��D�������������������·�Ӧ�����Ȼ����ķ�Ӧ����Ӧ�Ļ�ѧ����ʽΪ��2Fe+3Cl2![]() 2FeCl3��
2FeCl3��
(4)�����ж��������ŷŵ������У�װ��E������������Һ����������δ��Ӧ����������ֹ��Ⱦ����������������������Һ��Ӧ�����Ȼ��ơ��������ƺ�ˮ����Ӧ�����ӷ���ʽΪ��Cl2+2OH��=Cl��+ClO��+H2��
�ʴ�Ϊ��NaOH��Һ�� β����������ֹ������Ⱦ������Cl2+2OH��=Cl��+ClO��+H2��
��5������������ϢD�в�������H2O��g�����ҷ�Ӧ����Ϊ�ռ�D�в�����D��E֮�䣬�������ռ�װ���⣬����Ҫ���Ӹ���װ�ã��Գ�ȥˮ�������ʴ�Ϊ�����








