题目内容
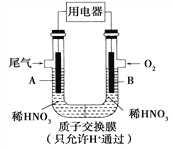
【题目】用如图所示装置探究铁粉在高温下与水蒸气反应的实验。

(1)仪器a的名称是__________________。
(2)干燥管C内盛放的药品是___________________。
(3)装置D中的现象是_________________________。
(4)写出铁在高温下与水蒸气反应的化学方程式:_________________________。
(5)当装置B的玻璃管中固体的质量增加16g时,生成H2在标准状况下的体积为______________。
【答案】 圆底烧瓶 无水CaCl2(或P2O5或碱石灰) 黑色固体变红,右端管壁有水珠 3Fe+4H2O(g) ![]() Fe3O4+4H2 22.4L
Fe3O4+4H2 22.4L
【解析】(1)铁粉在高温下与水蒸气反应,则A的作用为提供水蒸气,所用玻璃仪器为圆底烧瓶;(2)C中药品为碱石灰,可干燥氢气;(3)D中是氢气还原氧化铜得到铜和水,所以实验现象是硬质玻璃管中黑色固体变为红色,硬质玻璃管右端管壁有液滴生成;(4)高温下Fe与水蒸气反应生成四氧化三铁和氢气,反应方程式为3Fe+4H2O(g)![]() Fe3O4+4H2;(5)B中反应方程式为3Fe+4H2O(g)
Fe3O4+4H2;(5)B中反应方程式为3Fe+4H2O(g)![]() Fe3O4+4H2,所以B中增重的质量其实就是氧的质量,B的玻璃管中固体的质量增加16g,即氧元素的质量为16g,物质的量为1mol,氧元素来源于水,水中氢原子与氧原子的物质的量之比为2:1,所以氢原子的物质的量为2mol,则参加反应的水有1mol,根据关系式H2O~H2可知产生的氢气为1mol,在标况下的体积为22.4L。
Fe3O4+4H2,所以B中增重的质量其实就是氧的质量,B的玻璃管中固体的质量增加16g,即氧元素的质量为16g,物质的量为1mol,氧元素来源于水,水中氢原子与氧原子的物质的量之比为2:1,所以氢原子的物质的量为2mol,则参加反应的水有1mol,根据关系式H2O~H2可知产生的氢气为1mol,在标况下的体积为22.4L。

练习册系列答案
相关题目