题目内容
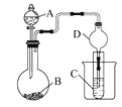
【题目】如图是两种溶液进行电解的装置。电极A是由金属M制成的,M的硝酸盐的化学式为M(NO3)2,B,C,D都是铂电极,P,Q是电池的两极,电路接通后,电极B上金属有M沉淀出来,

请回答下列问题:
(1)其中P是______极,B是______极。
(2)写出A极、B极、C极、D极上的电极反应式。
A极上电极反应式为____________________________________________________。
B极上电极反应式为____________________________________________________。
C极上电极反应式为____________________________________________________。
D极上电极反应式为____________________________________________________。
(3)当电路中通过2.4081022个电子时,B极上沉淀出1.28gM,则M的相对原子质量为__________。
(4)如果将电池的正负极交换,接入原电路通过1.2041022个电子时,则 B极上的电极反应式为____________________________________________,A极上析出______ g ______(填物质名称),甲池的总反应式为________________________________。
【答案】正 阴 M-2e- =M2+ M2+ + 2e- = M 4OH- - 4e- = 2H2O + O2↑ 2H+ + 2e- = H2↑ 64 4OH- - 4e- = 2H2O + 2↑ 0.64 铜 2Cu2+ + 2H2O ![]() 2Cu + O2↑ + 4H +
2Cu + O2↑ + 4H +
【解析】
电极A是由金属M制成的,M的硝酸盐的化学式为M(NO3)2,电路接通后,电极B上金属有M沉淀,则B电极M2++2e-=M,得电子,为电解池的阴极,则D为电解池的阴极,Q为电池的负极。
(1)电路接通后,电极B上金属有M沉淀出来,B电极得电子,作电解池的阴极,则B、D为电解池的阴极,A、C为电解池的阳极,P为电池的正极;
(2)A极为阳极,M失电子生成+2价的离子,则电极反应式为M-2e- =M2+;
B极为阴极,M2+得电子生成M,电极反应式为M2+ + 2e- = M;
C极为阳极,水失电子生成氧气和氢离子,电极反应式为2H2O - 4e- =4H++ O2↑;
D极为阴极,氢离子得电子生成氢气,电极反应式为2H+ + 2e- = H2↑;
(3)电路中通过2.408![]() 1022个电子时,即0.04mol电子,B极上析出的M的化合价由+2价变为0,其物质的量为0.02mol,其质量为1.28g,则摩尔质量=1.28g/0.02mol=64g/mol,相对原子质量为64;
1022个电子时,即0.04mol电子,B极上析出的M的化合价由+2价变为0,其物质的量为0.02mol,其质量为1.28g,则摩尔质量=1.28g/0.02mol=64g/mol,相对原子质量为64;
(4)将电池的正负极交换,B极为惰性电极,则做阳极,溶液中的水失电子生成氧气和氢离子,电极反应式为2H2O - 4e- =4H++ O2↑;电路通过1.204![]() 1022个电子时,即0.02mol,则有0.01molCu析出,即0.64g;则总反应式为2Cu2+ + 2H2O
1022个电子时,即0.02mol,则有0.01molCu析出,即0.64g;则总反应式为2Cu2+ + 2H2O ![]() 2Cu + 4H ++ O2↑。
2Cu + 4H ++ O2↑。