题目内容
【题目】天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷。
(1)工业上可用煤制天然气,生产过程中有多种途径生成CH4。
写出CO与H2反应生成CH4和H2O的热化学方程式
已知: CO(g)+H2O(g)![]() H2(g)+CO2(g) ΔH=-41kJ·mol-1
H2(g)+CO2(g) ΔH=-41kJ·mol-1
C(s)+2H2(g)![]() CH4(g) ΔH=-73kJ·mol-1
CH4(g) ΔH=-73kJ·mol-1
2CO(g)![]() C(s)+CO2(g) ΔH=-171kJ·mol-1
C(s)+CO2(g) ΔH=-171kJ·mol-1
(2)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中
通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式 。
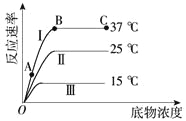
(3)天然气的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g)![]() 2CO(g)+2H2(g)。在密闭容器中通入物质的量浓度均为0.1mol·L-1的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图1所示,则压强P1 P2(填“大于”或“小于”);压强为P2时,在Y点:v(正) v(逆)(填“大于”、“小于”或“等于”)。 求Y点对应温度下的该反应的平衡常数K= 。(计算结果保留两位有效数字)
2CO(g)+2H2(g)。在密闭容器中通入物质的量浓度均为0.1mol·L-1的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图1所示,则压强P1 P2(填“大于”或“小于”);压强为P2时,在Y点:v(正) v(逆)(填“大于”、“小于”或“等于”)。 求Y点对应温度下的该反应的平衡常数K= 。(计算结果保留两位有效数字)

(4) 以二氧化钛表面覆盖CuAl2O4为催化剂,可以将CH4和CO2直接转化成乙酸。
①在不同温度下催化剂的催化效率与乙酸的生成速率如图2所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是 。
②为了提高该反应中CH4的转化率,可以采取的措施是 。
【答案】(1)CO (g)+3H2(g)![]() CH4(g)+ H2O(g) ΔH=-203kJ·mol-1
CH4(g)+ H2O(g) ΔH=-203kJ·mol-1
(2)2NH4HS+O2=2NH3·H2O+2S↓
(3)小于 大于 1.6mol2/L2
(4)①温度超过250oC时,催化剂的催化效率降低
②增大反应压强或增大CO2的浓度
【解析】试题分析:(1)根据盖斯定律,CO与H2反应生成CH4和H2O的热化学方程式为CO (g) + 3H2(g)![]() CH4(g) + H2O(g) ΔH=-203kJ·mol-1。(2)一定条件下向NH4HS溶液中通入空气,NH4HS能够与空气中的氧气反应得到单质硫从而使吸收液再生,其化学方程式为2NH4HS+O2=2NH3·H2O+2S↓。(3)反应CO2(g)+CH4(g)
CH4(g) + H2O(g) ΔH=-203kJ·mol-1。(2)一定条件下向NH4HS溶液中通入空气,NH4HS能够与空气中的氧气反应得到单质硫从而使吸收液再生,其化学方程式为2NH4HS+O2=2NH3·H2O+2S↓。(3)反应CO2(g)+CH4(g)![]() 2CO(g)+2H2(g)是一个熵增反应,增大压强,化学平衡向气体分子数减小的逆向进行,平衡转化率减小;而同温条件下,压强P1时的转化率大于压强P2时的转化率,因此压强P1小于P2。压强为P2时,在Y点,由于还未达到平衡状态,反应一直向正向进行着,因此v(正)大于v(逆)。由图1可知,在Y点对应温度下,该反应平衡转化率为0.8,则化学平衡常数的计算过程如下:
2CO(g)+2H2(g)是一个熵增反应,增大压强,化学平衡向气体分子数减小的逆向进行,平衡转化率减小;而同温条件下,压强P1时的转化率大于压强P2时的转化率,因此压强P1小于P2。压强为P2时,在Y点,由于还未达到平衡状态,反应一直向正向进行着,因此v(正)大于v(逆)。由图1可知,在Y点对应温度下,该反应平衡转化率为0.8,则化学平衡常数的计算过程如下:
CO2(g)+CH4(g)![]() 2CO(g)+2H2(g)
2CO(g)+2H2(g)
起始浓度(mol/L) 0.1 0.1 0 0
转化浓度(mol/L) 0.08 0.08 0.16 0.16
平衡浓度(mol/L) 0.02 0.02 0.16 0.16
平衡常数K=![]() mol2/L2
mol2/L2
(4)①250~300℃时,温度升高而乙酸的生成速率降低的原因是温度超过250oC时,催化剂的催化效率降低;②由于催化剂的催化效率在温度超过250时会降低,因此为了提高CH4的转化率,不能一味的升高温度,而是在催化剂催化效率最大时的温度条件下,采用增大反应压强或增大CO2的浓度的方式来提高CH4的转化率。

 小题狂做系列答案
小题狂做系列答案