题目内容
12.下列有机物的命名正确的是( )| A. | 1,1,2,2-四甲基戊烷 | B. | 3-甲基-1,3-丁二烯 | ||
| C. | 2,4,6-三硝基甲苯 | D. | 2-甲基-3-丁醇 |
分析 A、烷烃命名中出现1-甲基,说明选取的不是最长碳链;
B、二烯烃命名中碳碳双键位置一定时,选取距离支链最近的一端命名为1号碳;
C、硝基甲苯中甲基所处碳原子为1号碳;
D、醇类命名选取距离羟基最近的一端命名为1号碳.
解答 解:A、1,1,2,2-四甲基戊烷,主链选取错误,正确命名为:2,3,3-三甲基己烷,故A错误;
B、3-甲基-1,3丁二烯,链端选取错误,正确命名为:2-甲基-1,3-丁二烯,故B错误;
C、2,4,6-三硝基甲苯,符合硝基苯的命名原则,故C正确;
D、2-甲基3-丁醇,链端选取错误,正确命名为:3-甲基-2-丁醇,故D错误,故选C.
点评 本题主要考查的是烷烃的命名、烯烃的命名、醇类的命名,掌握各自的命名原则是解决本题的关键,难度不大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
3.湿化学法(NPP-法)制备纳米级活性氧化锌,可以用氧化锌粗品(含有FeO、Fe2O3、CuO杂质)为原料,采用酸浸出锌,经过多次净化除去原料中的杂质,然后沉淀获得碱式碳酸锌,最后焙烧获得活性氧化锌.其化学工艺流程如图:
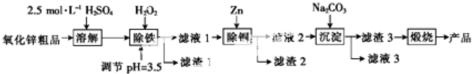
已知:溶液中Fe2+、Fe3+、Cu2+、Zn2+以氢氧化物的形式沉淀时的pH如表:
(1)实验室用98%浓H2SO4(ρ=1.84g/cm3)来配制100ml 2.5mol/L稀H2SO4所需的玻璃仪器有烧杯、胶头滴管、00mL容量瓶、量筒、玻璃棒.
(2)上述流程图中pH=12的Na2CO3溶液中阴离子的浓度由大到小的顺序为c(CO32-)>c(OH-)>c(HCO3-).
(3)滤渣1是Fe(OH)3(填化学式,下同),滤渣2是Cu、Zn.加入H2O2时发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)“沉淀”得到ZnCO3•2Zn(OH)2•H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为ZnCO3•2Zn(OH)2•H2O$\frac{\underline{\;450℃-500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.

已知:溶液中Fe2+、Fe3+、Cu2+、Zn2+以氢氧化物的形式沉淀时的pH如表:
| 离子 | 开始沉 淀的pH | 完全沉 淀的pH |
| Fe2+ | 6.4 | 8.4 |
| Fe3+ | 2.7 | 3.2 |
| Cu2+ | 5.2 | 6.7 |
| Zn2+ | 6.8 | 9.0 |
(2)上述流程图中pH=12的Na2CO3溶液中阴离子的浓度由大到小的顺序为c(CO32-)>c(OH-)>c(HCO3-).
(3)滤渣1是Fe(OH)3(填化学式,下同),滤渣2是Cu、Zn.加入H2O2时发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)“沉淀”得到ZnCO3•2Zn(OH)2•H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为ZnCO3•2Zn(OH)2•H2O$\frac{\underline{\;450℃-500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.
7.下列各组元素中,按从左到右的顺序,原子序数递增、元素的最高正化合价也递增的是( )
| A. | Na,Mg,Al,Si | B. | Na,Be,B,C | C. | P,S,Cl,Ar | D. | C,N,O,F |
4.下列热化学方程式书写正确的是(△H的绝对值均正确)( )
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol(燃烧热) | |
| B. | S(s)+O2(g)═SO2(g)△H=-269.8kJ/mol(反应热) | |
| C. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热) | |
| D. | 2NO2═O2+2NO△H=+116.2kJ/mol(反应热) |
2.对下列实验过程的评价,正确的是( )
| A. | 某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸根 | |
| B. | 某溶液中滴加BaCl2溶液,生成白色沉淀,证明一定含有SO42- | |
| C. | 验证烧碱溶液中是否含有Cl-,先加稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含Cl- | |
| D. | 某无色溶液滴入紫色石蕊试液显红色,该溶液一定显碱性 |
 .
.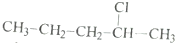

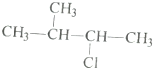
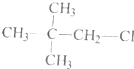
 利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同.根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同.根据峰值(信号)可以确定有机物分子中氢原子的种类和数目. 发生酯化反应的产物.
发生酯化反应的产物.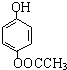 、
、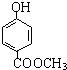 、
、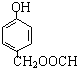 (其中之一).
(其中之一).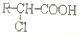

 .
.