��Ŀ����
��2014���Ϻ��а�У�����꼶���ϵ��п��Ի�ѧ�Ծ���
Ϊ��Ԥ����ȱ��֢�����ҹ涨ÿǧ��ʳ����Ӧ��40��50mg����ء�����ؾ����нϸߵ��ȶ��ԣ�����������Һ�У��������һ�ֽ�ǿ�����������ܸ�ijЩ��ԭ���������ɵ⣻�ڼ�����Һ�У�������ܱ��������������ǿ����������Ϊ���۵ĵ�ĺ������Ρ�
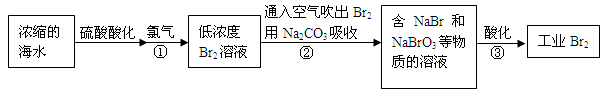
������1����ҵ��������ص��������£�
��1���⡢����غ�ˮ��Ϻ�ķ�ӦΪ��δ��ƽ����I2��KClO3��H2O��KH(IO3)2��KCl��Cl2�����÷���ʽ��ƽʱ��ϵ���ж��飬ԭ���� ��
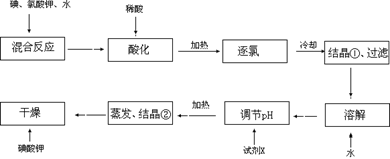
��2��X�Ļ�ѧʽΪ ��д�����Լ�X����pH�Ļ�ѧ����ʽ�� ��
��3�������У����ʡȥ���ữ���������ȡ������ᾧ�١����ˡ�������������ֱ�����Լ�X������Ӧ����Һ��pH���������������ʲô����Ӱ�죿 ��
������2����֪��KIO3��5KI��3H2SO4��3K2SO4��3I2��3H2O�� I2��2S2O32����2I����S4O62����
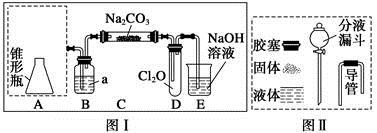
��4������ӵ�ʳ���еĵ�Ԫ�أ�ѧ�������õ������⻯�������������·�����Ӧ�������Ȼ�̼����ⵥ��ʱ������������������ ��
��5���ⶨ�ӵ�ʳ���е�ĺ�����ѧ������Ƶ�ʵ�鲽�����£�
a��ȷ��ȡw gʳ�Σ�����������ˮʹ����ȫ�ܽ⣻
b����ϡ�����ữ������Һ���������KI��Һ��ʹKIO3��KI��Ӧ��ȫ��
c���Ե���Ϊָʾ�����������ʵ���Ũ��Ϊ2.0��10��3mol��L��1��Na2S2O3��Һ10.0mLǡ�÷�Ӧ��
��ӵ�ʳ����Ʒ�еĵ�Ԫ�غ����� mg/kg���Ժ�w�Ĵ���ʽ��ʾ����
��6��ѧ�����ֶԴ�����NaCl������KIO3������������ʵ�飺
���Ʋ�ʵ���в�����ɫ����Ŀ���ԭ�������ӷ���ʽ��ʾ ��
�ڸ���ѧ������ʵ���������ѧ���ҵ�ʵ����������Ҫ���ۣ� ��
Ϊ��Ԥ����ȱ��֢�����ҹ涨ÿǧ��ʳ����Ӧ��40��50mg����ء�����ؾ����нϸߵ��ȶ��ԣ�����������Һ�У��������һ�ֽ�ǿ�����������ܸ�ijЩ��ԭ���������ɵ⣻�ڼ�����Һ�У�������ܱ��������������ǿ����������Ϊ���۵ĵ�ĺ������Ρ�
������1����ҵ��������ص��������£�

��1���⡢����غ�ˮ��Ϻ�ķ�ӦΪ��δ��ƽ����I2��KClO3��H2O��KH(IO3)2��KCl��Cl2�����÷���ʽ��ƽʱ��ϵ���ж��飬ԭ���� ��
��2��X�Ļ�ѧʽΪ ��д�����Լ�X����pH�Ļ�ѧ����ʽ�� ��
��3�������У����ʡȥ���ữ���������ȡ������ᾧ�١����ˡ�������������ֱ�����Լ�X������Ӧ����Һ��pH���������������ʲô����Ӱ�죿 ��
������2����֪��KIO3��5KI��3H2SO4��3K2SO4��3I2��3H2O�� I2��2S2O32����2I����S4O62����
��4������ӵ�ʳ���еĵ�Ԫ�أ�ѧ�������õ������⻯�������������·�����Ӧ�������Ȼ�̼����ⵥ��ʱ������������������ ��
��5���ⶨ�ӵ�ʳ���е�ĺ�����ѧ������Ƶ�ʵ�鲽�����£�
a��ȷ��ȡw gʳ�Σ�����������ˮʹ����ȫ�ܽ⣻
b����ϡ�����ữ������Һ���������KI��Һ��ʹKIO3��KI��Ӧ��ȫ��
c���Ե���Ϊָʾ�����������ʵ���Ũ��Ϊ2.0��10��3mol��L��1��Na2S2O3��Һ10.0mLǡ�÷�Ӧ��
��ӵ�ʳ����Ʒ�еĵ�Ԫ�غ����� mg/kg���Ժ�w�Ĵ���ʽ��ʾ����
��6��ѧ�����ֶԴ�����NaCl������KIO3������������ʵ�飺
| �������� | ʵ������ |
| ȡ1g������NaCl����3mLˮ�����Һ�� | ��Һ�ޱ仯 |
| ����5�ε�����Һ��1mL 0.1 mol��L��1 KI��Һ���� | ��Һ�ޱ仯 |
| Ȼ���ٵ���1��1mol��L��1��H2SO4���� | ��Һ����ɫ |
���Ʋ�ʵ���в�����ɫ����Ŀ���ԭ�������ӷ���ʽ��ʾ ��
�ڸ���ѧ������ʵ���������ѧ���ҵ�ʵ����������Ҫ���ۣ� ��
��1�������ֻ�ԭ�������ɡ�
��2��KOH�� KH(IO3)2��KOH=2KIO3��H2O
��3����Ӧ������������KOH��Ӧ����KClO�� KClO�ܽ�KIO3������KIO4�Ӷ����ܵõ�����ء�
��4��Һ��ֲ㣬�²�Һ������Ϻ�ɫ��
��5��1270/3W�� (423.33/W)��
��6����4I��+4H++O2��2I2+2H2O���� ������˹���KI��Һ����ʵ������ƫ��
��1���⡢����غ�ˮ��Ϻ�ķ�ӦΪ��δ��ƽ����I2��KClO3��H2O��KH(IO3)2��KCl��Cl2�����÷�Ӧ��������ԭ��Ӧ��������������ԭ��Ӧ�е���ת����Ŀ��ȣ��������ֻ�ԭ�������ɡ�����������Ķ��ٲ�ͬ����ƽʱ��ϵ���Ͳ�ͬ������ڸ÷���ʽ��ƽʱ��ϵ���ж��顣
��2�������ΪKH(IO3)2,�Ѿ������Һ�й��˳�����ϴ�Ӹɾ���Ȼ����ˮ�ܽ�õ�KH(IO3)2����Һ��Ҫ����ʽ�α�Ϊ����KIO3����Ҫ�Ӽ���������Һ��pHֵ��Ϊ�˲������µ����ʣ�����Ҫ��KOH���÷�Ӧ�ķ���ʽΪKH(IO3)2��KOH=2KIO3��H2O
��3����ӦI2��KClO3��H2O��KH(IO3)2��KCl��Cl2��������������KOH��Ӧ����KClO�� KClO�ܽ�KIO3������KIO4�Ӷ����ܵõ�����ء����²���ʧ�ܣ�ǰ��������
��4������ӵ�ʳ���еĵ�Ԫ�أ�ѧ�������õ������⻯�������������·�����ӦKIO3��5KI��3H2SO4��3K2SO4��3I2��3H2O������I2�����ܽ������Ȼ�̼���������ܽ���ˮ�У�ˮ�����Ȼ�̼�������ܣ�CCl4���ܶȱ�ˮ��I2�ܽ���CCl4�ж�ʹ��Һ����ɫ.���������Ȼ�̼����ⵥ��ʱ������������������Һ��ֲ㣬�²�Һ������Ϻ�ɫ��
��5���ɷ���ʽ�ù�ϵʽ��KIO3��3I2��6S2O32��.n(S2O32��)=2.0��10��3mol/L��0.010L=2.0��10��5mol.����n(KIO3)= 2.0��10��5mol��6=1/3��10��5mol.m(I)= (1/3��10��5mol)��127g/mol=127/3��10��5g=127/3��10��2mg.�����ڸüӵ�ʳ���е�ĺ���Ϊm(I)��m(��)= 127/3��10��2mg��W��10-3kg=1270/3W mg/kg��
��6���� ��ʳ������KIO3����ʵ���в�����ɫ����Ŀ����ǿ����е����������������°�I-����ΪI2���ʡ�4KI+2H2SO4��O2=2K2SO4��3I2��3H2O���ⵥ�������۱���ɫ���÷�Ӧ�����ӷ���ʽΪ4I��+4H+ +O2=2I2+2H2O�����ҵ�ʵ���м������KI��Һ������ѧ������ʵ��������֪�����е�����Ҳ�ᵼ�²���һ���ֵĵⵥ�ʡ�����ѧ���ҵ�ʵ��������ʵֵ��ƫ��

��ϰ��ϵ�д�
�����Ŀ