题目内容
实验室中制备HClO溶液的最好方法是将Cl2缓慢通入
| A.蒸馏水 | B.烧碱溶液 | C.纯碱溶液 | D.石灰石的悬浊液 |
D
解析试题分析:A.Cl2+H2O HCl+HClO。 由于产生的HCl会对平衡起抑制作用,所以制取的HCl浓度不大。B..Cl2+NaOH=NaCl+NaClO.不能得到HClO。C.由于酸性HCl>H2CO3>HClO ,所以会继续发生反应Na2CO3+ 2HCl=2NaCl+H2O+ CO2↑,使平衡正向移动,产生更多的HClO,因此比A好。但是溶液中可能有过量的Na2CO3,会导致HClO的含量低,而且纯度不高。D.在石灰石的悬浊液中存在沉淀溶解平衡CaCO3(s)
HCl+HClO。 由于产生的HCl会对平衡起抑制作用,所以制取的HCl浓度不大。B..Cl2+NaOH=NaCl+NaClO.不能得到HClO。C.由于酸性HCl>H2CO3>HClO ,所以会继续发生反应Na2CO3+ 2HCl=2NaCl+H2O+ CO2↑,使平衡正向移动,产生更多的HClO,因此比A好。但是溶液中可能有过量的Na2CO3,会导致HClO的含量低,而且纯度不高。D.在石灰石的悬浊液中存在沉淀溶解平衡CaCO3(s)  Ca2+(aq)+CO32-(aq), 由于在溶液中存在Cl2+H2O
Ca2+(aq)+CO32-(aq), 由于在溶液中存在Cl2+H2O HCl+HClO,且酸性HCl> H2CO3>HClO,所以会发生反应CO32-+2H+=CO2↑+H2O,使化学平衡和沉淀溶解平衡都正向移动,结果得到更多的产品,因为CaCO3难溶,所以不会引人过多的杂质。因此最好方法是将Cl2缓慢通入石灰石的悬浊液中。选项为D.
HCl+HClO,且酸性HCl> H2CO3>HClO,所以会发生反应CO32-+2H+=CO2↑+H2O,使化学平衡和沉淀溶解平衡都正向移动,结果得到更多的产品,因为CaCO3难溶,所以不会引人过多的杂质。因此最好方法是将Cl2缓慢通入石灰石的悬浊液中。选项为D.
考点:考查制备HClO的方法的选择。

 灵星计算小达人系列答案
灵星计算小达人系列答案将少量CO2通入下列溶液中,无沉淀产生的是
| A.Ba(OH)2溶液 | B.澄清石灰水 | C.氯化钡溶液 | D.漂白粉溶液 |
下列有关新制氯水的实验现象的描述错误的是 ( )
| A.新制氯水使碘化钾试纸呈蓝色 |
| B.向NaHCO3固体中加人新制氯水,有无色气体产生 |
| C.向FeC12溶液中滴加新制氯水,再滴加KSCN溶液,呈血红色 |
| D.在新制氯水中滴加AgN03溶液有白色沉淀生成 |
某同学利用如图所示装置进行实验,一段时间后,水沿导管缓慢上升。下列说法错误的是( )。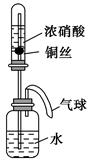
| A.实验过程中气球体积会发生变化 |
| B.广口瓶中液体的pH减小 |
| C.广口瓶中有化合反应发生 |
| D.试管中不可能发生分解反应 |
有一瓶无色气体可能含有CO2、HBr、NO2、HCl、SO2中的一种或几种。将此气体通入足量稀氯水中,恰好完全反应,得无色透明溶液,把此溶液分成两份,分别加入盐酸酸化了的BaCl2溶液和硝酸酸化了的AgNO3溶液,均出现白色沉淀,以下结论正确的是( )
| A.不能确定原气体中是否含有SO2 |
| B.原气体中肯定有HCl |
| C.原气体中肯定没有CO2 |
| D.原气体中肯定没有HBr、NO2 |
汉代器物上的颜料“汉紫”至今尚没有发现其自然存在的记载。20世纪80年代科学家进行超导材料研究时,偶然发现其成分为紫色的硅酸铜钡(化学式:BaCuSi2Ox,Cu为+2价),下列有关“汉紫”的说法中不正确的是( )。
| A.用盐的形式表示:BaSiO3·CuSiO3 |
| B.用氧化物形式表示:BaO·CuO·2SiO2 |
| C.易溶于强酸、强碱 |
| D.性质稳定,不易褪色 |
下列关于Cl2的说法正确的是( )
| A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂 |
| B.氯水光照时会放出Cl2,久置后只剩下水 |
| C.实验室制备Cl2时可用排饱和食盐水集气法收集Cl2 |
| D.Cl2能杀菌消毒,不需要进行尾气处理 |
我国成功地发射了嫦娥一号探测卫星,对月球土壤中14种元素的分布及含量进行探测等。月球的矿产资源极为丰富,仅月球表层5 cm厚的沙土中就含铁单质上亿吨,月球上的主要矿物有辉石[CaMgSi2O6]、斜长石[KAlSi3O8]和橄榄石[(MgFe)2SiO6]等,下列说法或分析不正确的是( )
| A.辉石、斜长石及橄榄石均属于硅酸盐 |
| B.斜长石的氧化物形式可表示为:K2O·Al2O3·6SiO2 |
| C.橄榄石中铁为+2价 |
| D.月球上有游离态铁是因为月球上铁的活动性比地球上铁的活动性弱 |