题目内容
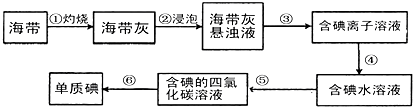
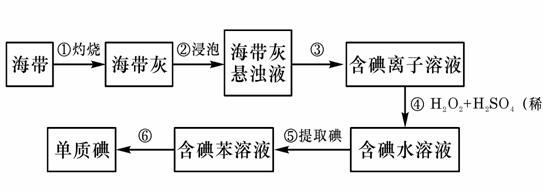
分海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验: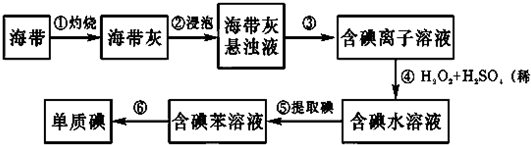
(1)步骤①应在
(2)步骤③的实验操作名称是
(3)步骤④反应的离子方程式是
分析:(1)根据实验操作步骤①灼烧来分析用到的实验仪器;
(2)分离固体和液体用过滤,分离互溶的两种液体用蒸馏;
(3)H2O2具有较强的氧化性,在酸性条件下可氧化碘离子.
(2)分离固体和液体用过滤,分离互溶的两种液体用蒸馏;
(3)H2O2具有较强的氧化性,在酸性条件下可氧化碘离子.
解答:解:(1)灼烧固体物质一般使用(瓷)坩埚,
故答案为:坩埚;
(2)步骤③是分离固体和液体,则实验操作为过滤,步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,
步骤⑥是利用互溶的两种液体的沸点不同来分离,则实验操作为蒸馏,
故答案为:过滤;蒸馏;
(3)碘离子在酸性条件下可被H2O2氧化成单质碘,H2O2被还原为水,反应的离子方程式为2I-+H2O2+4H+=I2+2H2O,
故答案为:2I-+H2O2+4H+=I2+2H2O.
故答案为:坩埚;
(2)步骤③是分离固体和液体,则实验操作为过滤,步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,
步骤⑥是利用互溶的两种液体的沸点不同来分离,则实验操作为蒸馏,
故答案为:过滤;蒸馏;
(3)碘离子在酸性条件下可被H2O2氧化成单质碘,H2O2被还原为水,反应的离子方程式为2I-+H2O2+4H+=I2+2H2O,
故答案为:2I-+H2O2+4H+=I2+2H2O.
点评:本题考查灼烧的实验,物质的分离方法,难度适中,注意从框图关系找出解题突破口.

练习册系列答案
相关题目
(12分)海带中含有丰富的碘。为了从海中提取碘,某研究性学习小组设计并进行了以下实验:
请填写下列空白:
⑴步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是 (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
| A.烧杯 | B.坩埚 | C.表面皿 | D.泥三角 E、酒精灯 F、干燥器 |
⑶步骤④反应的离子方程式是 。
⑷步骤⑤中,某学生选择用苯来提取碘的理由是 。
⑸请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法: 。