题目内容
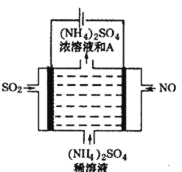
【题目】现有阳离子交换膜、阴离子交换膜、石墨电极和如图Z99所示电解槽。用氯碱工业中的离子交换技术原理,可电解Na2SO4溶液生产NaOH和H2SO4溶液。

下列说法正确的是( )
A.阳极反应式为2H++2e-===H2↑
B.从A口出来的是H2SO4溶液
C.a是阳离子交换膜,允许H+通过
D.Na2SO4溶液从E口加入
【答案】B
【解析】
试题分析:连接电源正极的是电解池的阳极,连接电源负极的是电解池的阴极,阳极是氢氧根离子放电产生的气体是氧气,同时生成氢离子,则阳极附近生成硫酸,则从A口出来的是H2SO4溶液,从E口进入的是稀硫酸,阴极是氢离子放电产生的气体是氢气,同时生成OH-,则阴极附近生成NaOH,从D口出来的是NaOH溶液,从G口进入的是稀硫酸。根据上述分析,阳极是氢氧根离子放电,阳极发生的反应为:2H2O-4e-═O2↑+4H+,A项错误;阳极是氢氧根离子放电产生的气体是氧气,同时生成氢离子,则阳极附近生成硫酸,则从A口出来的是H2SO4溶液,B项正确;C.在阳极室一侧放置阴离子交换膜,只允许通过阴离子,即a是阴离子交换膜,C项错误;D.NaOH在阴极附近生成,则Na2SO4溶液从G口加入,D项错误;答案选B。

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目