题目内容
下列各组物质的分类都正确的是(括号里的是类别)
| A.空气(混合物)、C2H5OH(醇)、H2SO4(离子化合物)、CO2(非电解质) |
| B.液氨(氢化物)、NH4Cl(铵盐)、HNO3(含氧酸)、NaOH(强电解质) |
| C.HCl(共价化合物)、CH3COOH(羧酸)、Na2O2(碱性氧化物)、CH3I(卤代烃) |
| D.NO2(酸性氧化物)、CH3CHO(有机物)、CO(有机物)、CH3COOCH3(酯) |
B
解析试题分析:A.H2SO4属于共价化合物;C.Na2O2属于过氧化物;D.CO是碳的氧化物,不属于有机物。
考点:物质的分类正误判断。

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案镁、铝、铁及其化合物在生产和生活中有广泛的应用。
(1)镁铝合金用在飞机制造业,现有3.90克镁铝合金溶于足量的2mol/L稀硫酸中生成0.2mol氢气,计算并确定镁铝合金中物质的量n(Mg): n(Al)= 。
(2)硫铁矿的主要成分为FeS2(假设杂质只含SiO2)是生产硫酸的原料。取某硫铁矿10g在足量的空气中煅烧(4FeS2+11O2→2Fe2O3+8SO2),充分反应后冷却,称得固体质量为7.4g(杂质SiO2不反应)。该硫铁矿中FeS2的质量分数为 。
(3)现有一定量的铁粉和铝粉组成的混合物跟100 mL稀硝酸充分反应,反应过程中无任何气体放出,往反应后的澄清溶液中逐渐加入4.00 mol·L-1的NaOH溶液,加入NaOH溶液的体积与产生沉淀的质量的关系如图所示(必要时可加热,忽略气体在水中的溶解):纵坐标中A点的数值是 。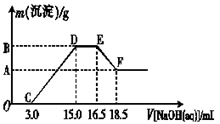
(4)炼铁厂生产的生铁常用于炼钢。取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况下)。
①计算此钢样粉末中铁和碳的物质的量之比为 (最简单的整数比)。
②再取三份不同质量的上述钢样粉末分别加到100mL相同浓度的稀H2SO4中,充分反应后,测得的实验数据如下表所示:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量(g) | 2.812 | 5.624 | 8.436 |
| 生成气体的体积(L)(标准状况) | 1.120 | 2.240 | 2.800 |
则该硫酸溶液的物质的量浓度为 。
③若在上述实验Ⅱ中继续加入m克钢样粉末,计算反应结束后剩余的固体质量为 g (保留3位小数)
从分类角度,下列说法正确的是
| A.水玻璃与硅胶均属于酸 |
| B.漂白液与漂粉精的主要成分均为钠盐 |
| C.NO2、SO3均属于酸性氧化物 |
| D.醋酸、一水合氨均属于弱电解质 |
全部属于纯净物的组合是( )
| A.福尔马林、白酒、食醋 | B.汽油、油脂、酚醛树脂 |
| C.石炭酸、盐酸、冰醋酸 | D.甘油、乙醇钠、氯仿 |
第二届青奥会“幸福之门”火炬用铝合金材料制造。铝合金属于
| A.盐 | B.氧化物 | C.纯净物 | D.混合物 |
下列说法中正确的是
A.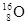 、 、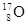 、 、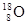 互为同素异形体 互为同素异形体 |
| B.O2与O3互为同位素 |
| C.CH3-CH2-OH与CH3-O-CH3互为同分异构体 |
D.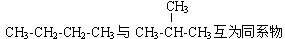 |
下列电离方程式,不正确的是
| A.KOH==K++OH- | B.CH3COOH==CH3COO- + H+ |
C.NH3·H2O NH4++OH- NH4++OH- | D.Na2CO3 ="=" 2Na++CO32- |
分类是化学研究的重要方法之一,下列有关说法中,正确的是
A.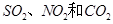 都属于酸性氧化物 都属于酸性氧化物 |
| B.甲烷和和一氯甲烷都属于烷烃 |
| C.HC1O是弱电解质,NaClO却属于强电解质 |
| D.在水溶液中能电离出H+的化合物都属于酸 |
分类法是一种行之有效、简单易行的科学方法。某同学用下表所示的形式对所学知识进行分类,其中甲与乙、丙、丁是包含关系。
| 选项 | 甲 | 乙、丙、丁 |
| ① | 常见干燥剂 | 浓硫酸、石灰石、碱石灰 |
| ② | 常见合金 | 不锈钢、青铜、生铁 |
| ③ | 基本营养物质 | 蛋白质、维生素、糖类 |
| ④ | 腐蚀品 | 浓硫酸、烧碱、硝酸 |
| ⑤ | 碱性氧化物 | 过氧化钠、氧化镁、氧化铁 |
| ⑥ | 弱电解质 | 醋酸、一水合氨、水 |
其中正确的组合是( )
A.①②③ B.④⑤⑥ C.②④⑥ D.①⑤⑥