题目内容
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g)△H=一92.6kJ/mol.实验测得起始、平衡时的有关数据如下表: ( )
2NH3(g)△H=一92.6kJ/mol.实验测得起始、平衡时的有关数据如下表: ( )
下列叙述不正确的是( )
A.容器①、②中反应的平衡常数相等
B.容器②中达平衡时放出的热量Q
C.平衡时,两个容器中NH3物质的量浓度均为2mol/L
D.若容器①体积为0.2L,则平衡时放出的热量大于23.15kJ
 2NH3(g)△H=一92.6kJ/mol.实验测得起始、平衡时的有关数据如下表: ( )
2NH3(g)△H=一92.6kJ/mol.实验测得起始、平衡时的有关数据如下表: ( )| 容器 | 起始各物质的物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.6 | 1.8 | 0.8 | Q(>0) |
A.容器①、②中反应的平衡常数相等
B.容器②中达平衡时放出的热量Q
C.平衡时,两个容器中NH3物质的量浓度均为2mol/L
D.若容器①体积为0.2L,则平衡时放出的热量大于23.15kJ
B
试题分析:A.衡常数只与温度有关,温度不变,对同一反应平衡常数不变,故A正确;
B.①容器中放出23.15kJ热量,则生成氨气的物质的量为: 23.15kJ/92.6(kJ/mol)×2=0.5mol,
X2(g)+3Y2(g)?2XY3(g)
起始(mol):1 3 0
转化(mol):0.25 0.75 0.5
平衡(mol):0.75 2.25 0.5
可知平衡时①容器中X2、Y2和XY3的物质的量分别为0.75mol、2.25mol和0.5mol,②与①为完全等效平衡,所以,平衡时②容器中X2、Y2和XY3的物质的量也分别为0.75mol、2.25mol和0.5mol,可知②的反应向逆反应方向进行,反应过程需要吸收热,故B错误;
C.由B计算可知此时XY3的物质的量浓度均为0.5mol/0.25L=2mol/L,将②按化学计量数比换算成左边与①对应的物质的物质的量相等,恒温恒容下,两平衡是完全等效平衡,平衡时各物质的浓度相等,故C正确;
D.若容器①体积为0.20L,增大压强平衡向正反应方向移动,放出热量多,故D正确。
故选B。
点评:本题考查化学平衡移动问题、等效平衡、反应热等问题,题目难度不大,注意B项根据计算分析,从等效平衡的角度判断反应进行的方向是解答该题的关键。

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
 CH3OH(g)
CH3OH(g)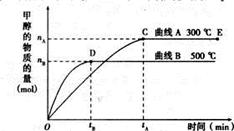

 = mol/(L·min)
= mol/(L·min)
 nW(g);ΔH ,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
nW(g);ΔH ,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
 C(g)+D(g)已达到平衡状态的现象是
C(g)+D(g)已达到平衡状态的现象是  4C (g) △H >0 达到平衡时,c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。试确定B的起始浓度c (B)的取值范围是 ;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是 。
4C (g) △H >0 达到平衡时,c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。试确定B的起始浓度c (B)的取值范围是 ;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是 。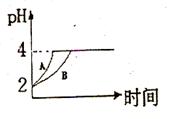
 pC(g)十qD(g),若其它条件都不变,只是在反应前是否加入催化剂,可得到如下两种v-t图象。下列判断正确的是( )
pC(g)十qD(g),若其它条件都不变,只是在反应前是否加入催化剂,可得到如下两种v-t图象。下列判断正确的是( )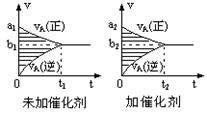
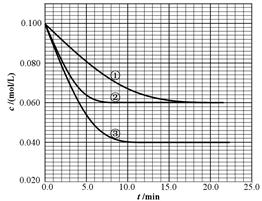
 B(g)+ C(g)分别在三种不同实验条件下进行,但起始浓度相同,均为c(A)=0.100mol/L、c(B)=0.020mol/L及c(C)=0.020mol/L。反应物A的浓度随时间的变化如下图所示:
B(g)+ C(g)分别在三种不同实验条件下进行,但起始浓度相同,均为c(A)=0.100mol/L、c(B)=0.020mol/L及c(C)=0.020mol/L。反应物A的浓度随时间的变化如下图所示: