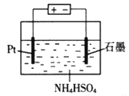
��Ŀ����
����Ŀ����1����һ��������ܱ������У��������»�ѧ��Ӧ��N2��g��+3H2��g��![]() 2NH3��g����H=-92.4 kJ/mol���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
2NH3��g����H=-92.4 kJ/mol���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t/K | 298 | 398 | 498 | ...... |
K/��mol/L��2 | 4.1��106 | K1 | K2 | ...... |
����������⣺
�ٱȽ�K1��K2�Ĵ�С��K1_______K2������>������=������<������
���ں��º�ѹ���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������_______������ţ���
A 2v��H2��������=3v��NH3�����棩
B 2v��N2��������=v��H2�����棩
C ������ѹǿ���ֲ���
D ���������ܶȱ��ֲ���
��2����ҵ���������صĻ�ѧ����ʽΪ��2NH3��g��+CO2��g��![]() CO��NH2��2��s��+H2O��l������T�棬���Ϊ4L���ܱ������У�ͨ��6molNH3��3molCO2����Ӧ�ﵽƽ��ʱ��c��NH3��=0.5mol��L��1����÷�Ӧ��ƽ�ⳣ��K=_______������ʱ����T���ƽ��ʱ������ѹǿ���䣬��������ɱ�������г���3molNH3�����ʱ��Ӧ��v��_______v��������>����<������=������
CO��NH2��2��s��+H2O��l������T�棬���Ϊ4L���ܱ������У�ͨ��6molNH3��3molCO2����Ӧ�ﵽƽ��ʱ��c��NH3��=0.5mol��L��1����÷�Ӧ��ƽ�ⳣ��K=_______������ʱ����T���ƽ��ʱ������ѹǿ���䣬��������ɱ�������г���3molNH3�����ʱ��Ӧ��v��_______v��������>����<������=������
��3����ǿ���Եĵ����ˮ��Һ�У����Բ������缫�����CO2�ɵõ�����ȼ�ϣ���ԭ����ͼ��ʾ��
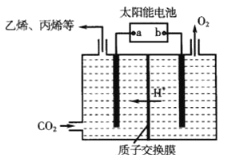
�ٸù���������ת����ʽ��Ҫ��_______��
�ڵ��ʱ��������ϩ�ĵ缫��Ӧʽ��_______��
���𰸡��� AD 16 �� ̫����ת��Ϊ���ܣ�����ת��Ϊ��ѧ�� 2CO2+12e-+12H+=C2H4+4H2O
��������
(1) �ٸ����ʱ��ж������ﷴӦ��Ũ�ȵı仯��Ȼ�����ƽ�ⳣ���жϣ�
�ڿ��淴Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�����ֵ�Ũ�ȡ��ٷֺ������ٱ仯���ݴ��жϣ�
(2)����ƽ�ⳣ��K=![]() ���㣻����Ũ����Qc��K�Ĺ�ϵ�жϷ�Ӧ����
���㣻����Ũ����Qc��K�Ĺ�ϵ�жϷ�Ӧ����
(3)��̫���ܵ���ǽ�̫����ת��Ϊ���ܣ����װ���ǽ�����ת��Ϊ��ѧ�ܣ�
��b�������ĵ��ص缫������������������Һ�е�����������ʧȥ���ӱ��������˵���缫Ϊ������
(1) �ٸ÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ,�����¶�,ƽ�����淴Ӧ�����ƶ�,������Ũ�ȼ�С,��Ӧ��Ũ������,����K1>K2���ʴ�Ϊ��>��
��A.2v(H2)(��)=3v(NH3)(��)��˵�����淴Ӧ������ȣ��÷�Ӧ�ﵽƽ��״̬����A��ȷ��B.2v(N2)(��)=v(H2)(��)����ʾ�������淴Ӧ���ʣ����������������ϵ��˵��û�дﵽƽ��״̬����B����C. ͬ��ͬѹ�����£�ѹǿʼ�ղ��䣬���ܸ���ѹǿ�ж�ƽ��״̬����C����D. ͬ��ͬѹ�£������ݻ�Ϊ�������������������䣬���ܶ�Ϊ�����������������ܶȱ��ֲ���ʱ�������ﵽƽ��״̬����D��ȷ���ʴ�Ϊ��AD��
(2) �¶Ȳ���,ƽ�ⳣ������,ƽ��ʱc(NH3)=0.5mol.L1��c(CO2)=0.25mol.L1��2NH3(g)+CO2(g)CO(NH2)2(s)+H2O(l)��ƽ�ⳣ��K=![]() =16���ʴ�Ϊ16��ͬ��ͬѹ��,����ȵ������ʵ���֮��,����ʱ����T����ƽ��ʱ������ѹǿ����,��������ɱ�������г���3molNH3,�������ΪV L,��
=16���ʴ�Ϊ16��ͬ��ͬѹ��,����ȵ������ʵ���֮��,����ʱ����T����ƽ��ʱ������ѹǿ����,��������ɱ�������г���3molNH3,�������ΪV L,��
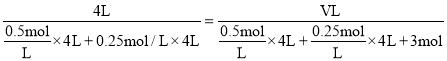 ��ã�V=8L,��ʱQ=
��ã�V=8L,��ʱQ=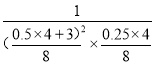 =20.48>16=K��,˵����ʱƽ�����������ƶ�,��V��<V�棬�ʴ�Ϊ<��
=20.48>16=K��,˵����ʱƽ�����������ƶ�,��V��<V�棬�ʴ�Ϊ<��
(3)��̫���ܵ���ǽ�̫����ת��Ϊ���ܣ����װ���ǽ�����ת��Ϊ��ѧ�ܣ��ʴ�Ϊ������ת��Ϊ���ܣ�����ת��Ϊ��ѧ�ܣ�
��b�������ĵ��ص缫������������������Һ�е�����������ʧȥ���ӱ��������˵���缫Ϊ���������ʱ������̼�õ����ӵõ���ϩ��ˮ������ʽΪ��2CO2+12e-+12H+=C2H4+4H2O���ʴ�Ϊ��2CO2+12e-+12H+=C2H4+4H2O��

 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�����Ŀ���������������������壬�Ǿ�����������ֲ���������ڼ���ʵ��֤������ʹ�ö�����������֪������������±���ʾ��
����ʽ | C12H10ClN3O |
�ṹ��ʽ |
|
��� | ��ɫ�ᾧ��ĩ |
�۵� | 170��172�� |
�ܽ��� | ������ˮ |
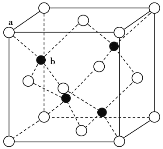
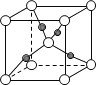
��1���������徧���У���ԭ�ӵ��ӻ���ʽΪ___��
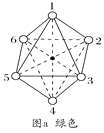
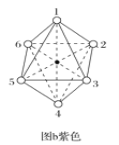
��2��������ɾ�ΪCoCl3��4NH3�������ֱ����ɫ����ɫ����֪��ɫ��������ڽ�ṹ�Գƣ�����ͼa��ͼb����Ԫ�ط��ű����ԭ�ӵ�λ��___��___��
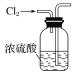
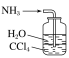
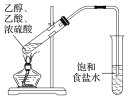
����Ŀ������ͼ��ʾװ�ü����Ӧ����ʱ�����ܴﵽĿ����
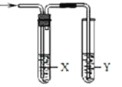
��X������װ�á�Y������װ�ã�
ʵ��Ŀ�� | �Լ�X | �Լ�Y | |
A | �����������л��е�NO2 | CCl4�Լ� | ʯ����Һ |
B | ����HI�л��е�HCl | ����NaCl��Һ | AgNO3��Һ |
C C | Ũ������MnO2������ȡ������ | NaOH��Һ | ����KI��Һ |
D | C2H5OH��ŨH2SO4������170����ȡ����ϩ | NaOH��Һ | Br2��CCl4��Һ |
A.AB.BC.CD.D
����Ŀ����ѧ��һ����ʵ��Ϊ�����Ŀ�ѧ��
(1)������ʵ��װ����ɶ�Ӧ��ʵ��(����������ȥ)���ܴﵽʵ��Ŀ�ĵ���________(����ĸ)��
A | B | C | D |
|
|
|
|
�������� | ����NH3 | ʯ�͵ķ��� | ��ȡ�������� |
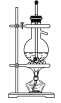
(2)Ϊ��ȥ�����е�MgCl2��CaCl2��Na2SO4�Լ���ɳ�����ʣ�ijͬѧ�����һ���Ʊ����ε�ʵ�鷽������������(���ڳ������Լ��Թ���)��
![]()
�ٵ�����������������____________��
��������������˳��ߵ����Ƿ���ʵ��������Ӱ�죿________(������Ӱ����������Ӱ����)��
�۵������������貣��������������____________��