题目内容
【题目】检验某未知溶液中是否含有SO42—,下列操作最合理的是( )
A. 先加稀硫酸酸化,再加氯化钡溶液
B. 加入氯化钡溶液
C. 加入盐酸酸化的氯化钡溶液
D. 先用盐酸酸化,若有沉淀,则过滤,滤液中再加氯化钡溶液
【答案】D
【解析】
A. 先加稀硫酸酸化,引入了SO42-,故A错误;
B. 加入氯化钡溶液,可能产生碳酸钡白色沉淀,不能说明SO42-肯定是存在,故B错误;
C. 加入盐酸酸化的氯化钡溶液,可能产生氯化银白色沉淀,故C错误;
D. 检验某溶液中是否含有SO42-的方法:先用盐酸酸化(若有沉淀,过滤),再加氯化钡溶液,若有白色沉淀,说明有SO42-,故D正确;
故选D。

练习册系列答案
相关题目
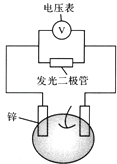
【题目】留心处处皆学问.从生活出发进行科学探究,可以获得自信,形成正确的思维方式.甲、乙两位同学一起合作设计完成了水果电池的实验(如图),测得数据如下
实验序号 | 电极材料 | 水果种类 | 电极间距离/cm | 电压/mV |
1 | 锌铜 | 菠萝 | 3 | 900 |
2 | 锌铜 | 苹果 | 3 | 650 |
3 | 锌铜 | 柑橘 | 3 | 850 |
4 | 锌铜 | 西红柿 | 3 | 750 |
5 | 锌铝 | 菠萝 | 3 | 650 |
6 | 锌铝 | 苹果 | 3 | 450 |
对甲同学提出的问题,乙同学的解释不正确的是( )
甲同学 | 乙同学 | |
A | 实验6中负极电极反应式如何写? | Al﹣3e﹣=Al3+ |
B | 实验1,5中电流方向为什么相反? | 1中锌为负极,电流由铜经导线流向锌,5中铝为负极,铝失去电子,电流由锌经导线流向铝 |
C | 水果电池的电压与哪些因素有关? | 只跟水果的类型有关 |
D | 实验中发光二极管不亮,如何使它亮起来 | 可用铜锌作电极,用菠萝作介质,并将多个此电池串联起来 |
A.A
B.B
C.C
D.D
