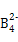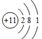题目内容
A、B、C、D、E、F元素是原子序数依次增大的6种短周期元素。已知A是短周期元素中原子半径最小的元素,A和B形成的18电子的化合物X常用作火箭的燃料,C原子最外层电子数与核外电子总数之比为3∶4,E与C同主族,D和C可以形成原子个数比为1∶1和2∶1的两种离子化合物。
据此回答下列问题:
(1)D和C形成1∶1的化合物中阴阳离个数比为____________。
(2)化合物X的结构式为____________。1 mol气态X在适量C2中燃烧,生成B2和气态A2C, 放出534 kJ的热量,1 mol液态A2C完全汽化需吸收44 kJ热量。请写出气态X在C2中燃烧生成B2和液态A2C时的热化学方程式_____________________________________
(3)某化合物由上述6种元素中的3种元素组成,为常见家用消毒剂的主要成分,其中化学键类型为__________________;该化合物水溶液不呈中性的原因是(用离子方程式表示)__________________________________,该化合物可以通过电解D和F形成化合物的水溶液获得,电解时反应的化学方程式为_________________________________
(4)写出一个可以证明C的非金属性大于E的化学反应方程式:_____________________________________________。
据此回答下列问题:
(1)D和C形成1∶1的化合物中阴阳离个数比为____________。
(2)化合物X的结构式为____________。1 mol气态X在适量C2中燃烧,生成B2和气态A2C, 放出534 kJ的热量,1 mol液态A2C完全汽化需吸收44 kJ热量。请写出气态X在C2中燃烧生成B2和液态A2C时的热化学方程式_____________________________________
(3)某化合物由上述6种元素中的3种元素组成,为常见家用消毒剂的主要成分,其中化学键类型为__________________;该化合物水溶液不呈中性的原因是(用离子方程式表示)__________________________________,该化合物可以通过电解D和F形成化合物的水溶液获得,电解时反应的化学方程式为_________________________________
(4)写出一个可以证明C的非金属性大于E的化学反应方程式:_____________________________________________。
(1)1∶2
(2)NHHNHH N2H4(g)+O2(g)=N2(g)+2H2O(l) ΔH=-622 kJ/mol
(3)离子键和共价键 ClO-+H2O??HClO+OH- NaCl+H2O NaClO+H2↑
NaClO+H2↑
(4)O2+2H2S=2H2O+2S
(2)NHHNHH N2H4(g)+O2(g)=N2(g)+2H2O(l) ΔH=-622 kJ/mol
(3)离子键和共价键 ClO-+H2O??HClO+OH- NaCl+H2O
 NaClO+H2↑
NaClO+H2↑(4)O2+2H2S=2H2O+2S
根据题意可推出A、B、C、D、E、F分别为H、N、O、Na、S、Cl。(1)D元素的氧化物为氧化钠和过氧化钠,两种化合物中阴阳离子个数比均为1∶2。(2)根据题意可知化合物X为N2H4,结构式为NHHNHH,根据题意可写出热化学方程式:① N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-534 kJ· mol-1,② H2O(g)=H2O(l) ΔH=-44 kJ· mol-1。根据盖斯定律①+2×②可得:N2H4(g)+O2(g)=N2(g)+2H2O(l) ΔH=-622 kJ· mol-1。
(3)由上述6种元素中的3种元素组成的常见家用消毒剂的主要成分为NaClO,由于ClO-的水解,NaClO溶液呈碱性。制备的化学方程式为NaCl+H2O NaClO+H2↑。
NaClO+H2↑。
(4)证明氧的非金属性大于硫可用反应O2+2H2S=2H2O+2S
(3)由上述6种元素中的3种元素组成的常见家用消毒剂的主要成分为NaClO,由于ClO-的水解,NaClO溶液呈碱性。制备的化学方程式为NaCl+H2O
 NaClO+H2↑。
NaClO+H2↑。(4)证明氧的非金属性大于硫可用反应O2+2H2S=2H2O+2S

练习册系列答案
相关题目

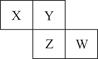
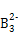 、A2
、A2