题目内容
【题目】I、(1)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式:____________________;:如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打,此时最好用含Al(OH)3的胃药(如胃舒平),它与胃酸反应的离子方程式为:______________________
(2)有一包白色粉末,其中可能含有NaCI、Ba(NO3)2、CuSO4、Na2CO3,现做以下实验:
① 将部分粉末加入水中,振荡,有白色沉淀生成,过滤,滤液呈无色
② 向①中的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生
③ 取少量②的溶液,滴入稀硫酸,有白色沉淀产生
试根据上述实验现象判断,原白色粉末中一定含有的物质是_____________,可能含有的物质是__________(以上物质均写化学式),写出第①步中反应的化学方程式为__________________第②步反应中离子方程式为____________________
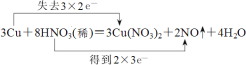
II、根据反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,回答下列问题:
(1)还原产物是__________
(2)氧化剂与还原剂的物质的量之比是____________
(3)用双线桥标上电子转移的方向和数目_________________
【答案】Ⅰ.(1)HCO3-+H+=CO2↑+H2O(2分);
Al(OH)3+3H+=Al3++3H2O(2分)
(2)Ba(NO3)2;Na2CO3;NaCl
Ba(NO3)2+Na2CO3=2NaNO3+BaCO3↓(2分);
BaCO3+2H+=CO2↑+H2O+Ba2+(2分)
II.(1)NO(2分)(2)2:3(2分)
(3)
【解析】
试题分析:I、(1)胃液成分为盐酸小苏打(NaHCO3),能与盐酸反应, HCO3-+H+=CO2↑+H2O ;Al(OH)3为两性化合物,能够与盐酸反应:Al(OH)3+3H+=Al3++3H2O;(2)①有白色沉淀,溶液无色,一定含有Ba(NO3)2和Na2CO3,一定不含CuSO4,向①中的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生,沉淀一定为碳酸盐;取少量②的溶液,滴入稀硫酸,有白色沉淀产生,沉淀为硫酸钡;一定含有的物质是Ba(NO3)2 和Na2CO3;可能含有的物质是NaCl;第①步中反应的化学方程式为Ba(NO3)2 + Na2CO3 = 2NaNO3+BaCO3 ↓;第②步反应中离子方程式BaCO3 +2H+ = CO2↑+H2O+Ba2+;
II、3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;Cu失电子,做还原剂,HNO3得电子,做氧化剂;但是8HNO3参加反应只有2 HNO3被还原,氧化剂与还原剂的物质的量之比是2:3;还原产物NO;
用双线桥标上电子转移的方向和数目,见答案。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列实验操作能达到实验目的的是( )
选项[ | 实验目的 | 实验操作 |
A | 除去CO2中少量的CO | 点燃 |
B | 除去CuSO4溶液中的少量FeSO4 | 加入足量的铜粉 |
C | 鉴别澄清石灰水和NaOH溶液 | 加入稀盐酸 |
D | 鉴别硬水和软水 | 加入肥皂水 |