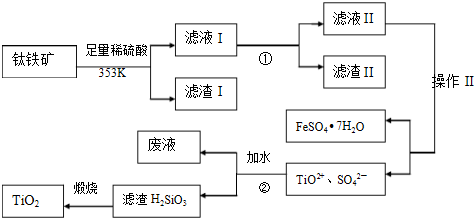
题目内容
将硫酸亚铁晶体(FeSO4·7H2O)放入图Ⅰ 的干燥试管A里隔绝空气加强热,充分反应后,试管A里残留固体甲,试管B内得到无色液体乙。取出甲放在图Ⅱ的石英管C中部,连接好其他部分的仪器后,开启旋塞K,逐滴滴下乙醇使C管左部石棉绒(一种纤维状硅酸盐材料,很稳定,不燃烧)浸润吸足,关闭K。然后加热5分钟左右,加热过程中还较快地开启或关闭旋塞K以补充乙醇并使之渗入石棉绒里,同时观察到甲的颜色由红棕色逐渐变为黑色。反应停止后,取试管E中的液体0.5 mL逐渐加入到图Ⅲ盛有新配制的银氨溶液的试管F里,水浴加热,不久观察到试管内壁出现光亮如镜的物质。回答下列问题:?
(1)写出图Ⅰ干燥试管里隔绝空气强热硫酸亚铁晶体的化学方程式:?
。?
(2)根据反应原理请你评价图 Ⅰ 实验装置的主要缺点是什么??
。?
(3)试管B中所得液体乙的名称是 ;如何用实验确证乙的阴离子? 。?
(4)怎样检验图Ⅱ装置的气密性? 。
(5)管D在此处的主要作用是 。
(6)根据图Ⅲ试管F中的现象得出的结论是 ;写出C管中发生反应的化学方程式___ 。?
(1)2FeSO4·7H2O![]() Fe2O3 + SO2↑+ SO3 + 14H2O?
Fe2O3 + SO2↑+ SO3 + 14H2O?
(2)缺少尾气处理装置?
(3)硫酸(或硫酸与亚硫酸) 取少量液体于小试管中,加入氯化钡溶液,待产生白色沉淀后再加入稀盐酸,若沉淀不消失说明阴离子是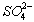
(4)关闭活塞K,将试管E中导管的末端浸入水中,微热石英管C,E中导管内有气泡产生时,停止加热,导管中出现一段水柱,说明装置不漏气?
(5)防止倒吸(起安全瓶的作用)?
(6)在石英管C中发生反应生成乙醛,即乙醇能被Fe2O3氧化?
3CH3CH2OH + Fe2O3![]() 2Fe + 3CH3CHO + 3H2O?
2Fe + 3CH3CHO + 3H2O?
解析:(1)FeSO4·7H2O隔绝空气加强热反应为?
2FeSO4·7H2O![]() Fe2O3+SO2↑+ SO3 + 14H2O,则B中得到的物质为SO3,A中剩余物质为Fe2O3。在C管中反应为3CH3CH2OH + Fe2O3
Fe2O3+SO2↑+ SO3 + 14H2O,则B中得到的物质为SO3,A中剩余物质为Fe2O3。在C管中反应为3CH3CH2OH + Fe2O3![]() 2Fe + 3CH3CHO + 3H2O。E中液体为CH3CHO。?
2Fe + 3CH3CHO + 3H2O。E中液体为CH3CHO。?
(2)图Ⅰ中由于生成SO2而污染空气,应加尾气处理装置。?
(3)试管B中得到的是H2SO4或H2SO3,欲确定B中得到阴离子,即确定是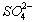 或
或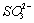 ,则应加BaCl2,再加稀盐酸,若沉淀不消失说明是有
,则应加BaCl2,再加稀盐酸,若沉淀不消失说明是有 。?
。?
(4)装置Ⅱ有两个气体出口,故必须先关闭一个,即K,然后进行气密性检验。?
(5)C处产生乙醛气体易溶于水,故D处装置应为防止倒吸。?
(6)据图Ⅲ生成了CH3CHO。