题目内容
【题目】某废液中含有Fe3+、Cu2+、Ag+金属离子,某研究小组设计的处理方案如下(假如各步骤所加试剂都过量):
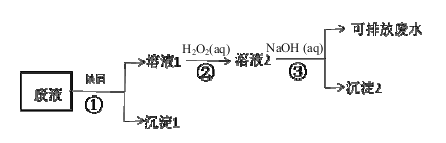
(1)沉淀1的主要成分是_________(用元素符号表示),沉淀2化学式为___ ___。
(2)步骤②发生反应的离子方程式 。
【答案】(1)Ag、Cu、Fe(2分);Fe(OH)3(1分)
(2)2Fe2++H2O2+2H+=2Fe3++2H2O(2分)
【解析】
试题分析:(1)废液中含有Fe3+、Cu2+、Ag+金属离子,加入铁屑,发生反应为Fe+2Ag+=Fe2++2Ag、Fe+2Fe3+=3Fe2、Fe+Cu2+=Fe2++Cu,所以沉淀1为Ag、Cu、 Fe;向含Fe2+的溶液中加入H2O2,发生氧化还原反应生成Fe3+,加入NaOH生成Fe(OH)3 红褐色沉淀,则沉淀2为Fe(OH)3。
(2)Fe2+具有还原性,H2O2具有氧化性,两种发生氧化还原反应生成Fe3+和水,根据得失电子守恒、电荷守恒和原子守恒配平,则步骤②发生反应的离子方程式为2Fe2++ H2O2 +2 H+ = 2Fe3++2H2O。

练习册系列答案
相关题目