题目内容
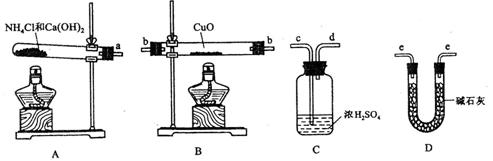
根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量Ar(Cu)(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),同时生成有一种对环境无害的气体,由此计算Ar(Cu)。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
请回答下列问题:
(1)检验装置A的气密性的方法是
。
(2)装置A中发生反应的化学方程式为 ,氨气还原炽热氧化铜的化学方程式为 。
(3)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→ 。
(4)在本实验中,若测得m(CuO)=ag,m(H2O)=bg,则Ar(Cu)= 。
(5)在本实验中,使测定结果Ar(Cu)偏大的是_______________(填序号)。
①CuO未完全起反应 ②CuO不干燥 ③CuO中混有不反应的杂质
④碱石灰不干燥 ⑤NH4C1与Ca(OH)2混合物不干燥
(6)在本实验中,还可通过测定______________和_____________,或_______________和_______________达到实验目的。
(共12分)(1)将装置末端的导管放入盛有水的水槽中,双手捂住试管,导管口有气泡冒出,松开双手,导管内有一段水柱上升,则装置气密性良好。(2分)
(2)2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O 2NH3+3CuO
CaCl2+2NH3↑+2H2O 2NH3+3CuO![]() 3Cu+3H2O+N2↑ (各1分)
3Cu+3H2O+N2↑ (各1分)
(3)a→e→e→b→b→e→e(全对才得分, 2分) (4)18a/b-16(2分)
(5)①③(各1分,错1个倒扣1分,扣完为止)
(6)m(CuO)和m(Cu),m(Cu)和m(H2O) (各1分)
解析:

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
 (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H20),由此计算
(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H20),由此计算 (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量
(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量 m(H20),由此计算
m(H20),由此计算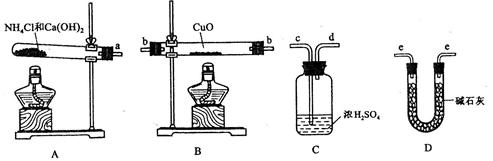
 的是_______________ (填序号);
的是_______________ (填序号); 干燥
干燥 _____和_______________达到实验目的。
_____和_______________达到实验目的。 (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H20),由此计算
(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H20),由此计算