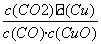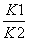��Ŀ����
I�����¶�ΪTʱ����2.0 L�����ܱ������г���1.0 mol A��1.0 mol B��������ӦA(g)��B(g)  C(g)��һ��ʱ���ﵽƽ�⡣�ⶨ�ò������ݼ��±���
C(g)��һ��ʱ���ﵽƽ�⡣�ⶨ�ò������ݼ��±���
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
�ش��������⣺
(1)��Ӧǰ5 s��ƽ����Ӧ����v(A) ��____________
(2)�¶�ΪTʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ����
(3)�����¶ȣ�ƽ��ʱc(A)��0.41 mol��L��1����Ӧ�Ħ�H ���� ��>0�� �� ��<0����
(4)��ͬ�¶��£���ʼʱ�������г���0.2 mol A��0.2 mol B��1.0 mol C����Ӧ�ﵽƽ��ǰ����Ӧ����v�� v��������>�� �� ��<����
(5)���д�ʩ������Ӧ���ʣ���ƽ��������Ӧ�����ƶ��� ��
a����ʱ�����A���� b���ʵ������¶�
c������B��Ũ�� d��ѡ���Ч����
II��NO��NO2�dz������������H2��CO����ԭNO�ɴﵽ������Ⱦ��Ŀ�ġ�
��֪��2NO(g) = N2(g) + O2(g) ��H = -180.5kJ��mol-1
2H2O(l) = 2H2(g) + O2(g) ��H = +571.6kJ��mol-1
����H2����ԭNO������Ⱦ���Ȼ�ѧ����ʽ��
I.��1��0.015 mol/(L��s) ��2�� 0.625
��3��< 0 ��4��< ��5��c
II. 2H2(g) + 2NO(g) = N2(g) + 2H2O(l) ��H = -752.1kJ��mol-1 ���д������֣�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�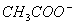 )��C(Na+)
)��C(Na+)  2C���磩�ﵽƽ��ı�־��
2C���磩�ﵽƽ��ı�־��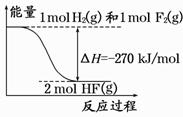
 2B(g) ��C(g)
2B(g) ��C(g) 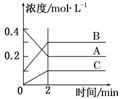
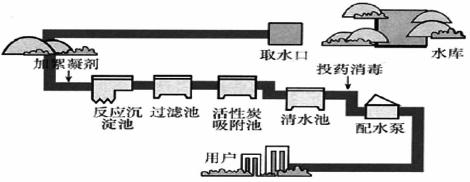
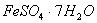 �dz��õ�������������ˮ����������__________�������ѧʽ����
�dz��õ�������������ˮ����������__________�������ѧʽ����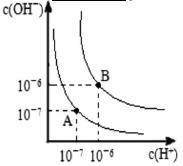
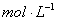 ��NaOH��Һ�У���ˮ�������c��H+��=________
��NaOH��Һ�У���ˮ�������c��H+��=________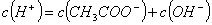
 CO2(g)��Cu(s)�ͷ�Ӧ�ڣ�H2(g)��CuO(s)
CO2(g)��Cu(s)�ͷ�Ӧ�ڣ�H2(g)��CuO(s)