题目内容
19.下列关于原电池叙述不正确的是( )| A. | 相对活泼的金属做负极 | B. | 原电池是把化学能转换为电能 | ||
| C. | 正极发生还原反应 | D. | 电流从正极经导线流向负极 |
分析 原电池是把化学能转化为电能的装置,原电池放电时,负极上失电子发生氧化反应,正极上得电子发生还原反应,电流从正极经导线流向负极,据此分析解答.
解答 解:A、原电池中,失电子的电极是负极,活泼金属不一定是负极,如Al-Cu-浓硝酸原电池中,Cu为负极,故A错误;
B、原电池是把化学能转化为电能的装置,故B正确;
C、原电池放电时,负极上失电子发生氧化反应,正极上得电子发生还原反应,故C正确;
D、原电池放电时,电流从正极经导线流向负极,和电子的移动方向相反,故D正确.
故选A.
点评 本题考查了原电池的有关知识,难度不大,根据原电池工作原理及原电池的构成条件分析判断即可.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案
相关题目
9.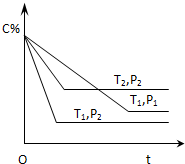 已知某可逆反应:mA(气)+nB(气)?xC(气)△H=QkJ•mol-1,在密闭容器中进行,如图表示反应在不同时间t,温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则( )
已知某可逆反应:mA(气)+nB(气)?xC(气)△H=QkJ•mol-1,在密闭容器中进行,如图表示反应在不同时间t,温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则( )
 已知某可逆反应:mA(气)+nB(气)?xC(气)△H=QkJ•mol-1,在密闭容器中进行,如图表示反应在不同时间t,温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则( )
已知某可逆反应:mA(气)+nB(气)?xC(气)△H=QkJ•mol-1,在密闭容器中进行,如图表示反应在不同时间t,温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则( )| A. | T1>T2,P1>P2,m+n>x,Q>0 | B. | T1>T2,P1<P2,m+n<x,Q<0 | ||
| C. | T1>T2,P1<P2,m+n<x,Q>0 | D. | T1<T2,P1>P2,m+n>x,Q<0 |
14.下列措施不能加快化学反应速率的是( )
| A. | 提高反应物的浓度 | B. | 使用合适的催化剂 | ||
| C. | 降低温度 | D. | 增大压强 |
4.X、Y、Z、W四种金属单质①X、Y形成的原电池中,X做负极;②Z、W形成的原电池中Z附近有气泡;③Y、W分别与稀盐酸反应,Y反应较快,则四种金属活泼性由强到弱的顺序是( )
| A. | X、Y、W、Z | B. | X、Y、Z、W | C. | W、Z、X、Y | D. | Z、W、X、Y |
11.根据下表部分短周期元素的原子半径及主要化合价信息回答以下问题:
(1)E与氢形成的化合物由两种分别是H2O、H2O2,其中心原子的杂化方式分别是sp3、sp3.
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是Al(OH)3+3H+═Al3++3H2O.
(3)实验室中制取H单质反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
| 元素 | A | B | C | D | E | F | G | H |
| 原子半径(nm) | 0.130 | 0.118 | 0.090 | 0.102 | 0.073 | 0.154 | 0.037 | 0.099 |
| 主要化合价 | +2 | +3 | +2 | +6,-2 | -2 | +1 | +1 | +7,-1 |
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是Al(OH)3+3H+═Al3++3H2O.
(3)实验室中制取H单质反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
 .
.
 .
.