题目内容
下列叙述中能表明金属甲的活动性比金属乙的活动性强的是( )。
| A.在氧化还原反应中,甲失电子数比乙多 |
| B.同价态阳离子甲比乙氧化性强 |
| C.甲能跟盐酸反应放出H2而乙可与冷水反应产生H2 |
| D.甲、乙与H2SO4溶液形成原电池,乙上冒气泡 |
D
解析

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
市售的食品包装中常带有一小包铁粉,并标有“吸氧剂”字样,这是利用了铁粉的
| A.氧化性 | B.还原性 | C.吸水性 | D.导电性 |
将3.5gFe、Mg合金投入到一定量的硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体V L(HNO3被还原为NO和NO2);若向反应后的溶液中加入足量的氢氧化钠溶液,待金属元素全部沉淀后,再将沉淀过滤、洗净、干燥后称量质量为8.6g。则收集到的气体体积V值可能为
| A.1.12 | B.5.34 | C.7.26 | D.8.23 |
将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是
| A.与NaOH反应的氯气一定为0.3 mol |
| B.n(Na+):n(Cl-)可能为7:3 |
| C.若反应中转移的电子为n mol,则0.15<n<0.25 |
| D.n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 |
下列叙述正确的是( )
| A.金属元素的原子只有还原性,离子只有氧化性 |
| B.用乙烷(CH3CH3)或乙烯(CH2=CH2)制一氯乙烷(CH3CH2Cl)的反应类型相同 |
| C.煤油是通过煤干馏获得,可用作燃料和保存少量金属钠 |
D.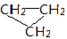 和CH3-CH=CH2互称为同分异构体 和CH3-CH=CH2互称为同分异构体 |
氢化亚铜(CuH)是一种不稳定的物质,能在氯气中燃烧,也能与酸反应。用CuSO4溶液和“某物质”在40~50 ℃时反应可生成CuH。下列叙述中错误的是 ( )。
| A.“某物质”具有还原性 |
| B.CuH与盐酸反应可能产生H2 |
| C.CuH与足量稀硝酸反应:CuH+3H++NO3-=Cu2++NO↑+2H2O |
| D.CuH在氯气中燃烧:CuH+Cl2=CuCl+HCl |
取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生8 960 mL的NO2气体和672 mL N2O4的气体(都已折算到标准状态),在反应后的溶液中加足量的氢氧化钠溶液,生成沉淀质量为17.02 g。则x等于( )
| A.8.64 g | B.9.20 g |
| C.9.00 g | D.9.44 g |
下列叙述正确的是( )
| A.在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 |
| B.元素由化合态变成游离态时,它可能被氧化,也可能被还原 |
| C.元素的原子得失电子后,一定形成8电子的稳定结构 |
| D.有单质参加或生成的反应一定属于氧化还原反应 |
根据反应:2H2S+O2=2S↓+2H2O,Na2S+I2=2NaI+S↓,4NaI+O2+2H2SO4=2I2+2Na2SO4+2H2O,下列物质的氧化性强弱判断正确的是( )
| A.O2>I2>S | B.H2S>NaI>H2O |
| C.S>I2>O2 | D.H2O>NaI>H2S |