题目内容
(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)醋酸钠水溶液PH 7 ,(填“>”、“=”、“<”)原因是(用离子方程式表示):______。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)氯化铵溶液中滴加适量氨水,至溶液呈中性,则c(Cl-) c(NH4+)(填“>”、“=”、“<”)。(4)在25℃下,某浓度Na2CO3溶液中由水电离出来c(OH-)=1×10-6 mol/L,则此溶液的PH值为
(2)醋酸钠水溶液PH 7 ,(填“>”、“=”、“<”)原因是(用离子方程式表示):______。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)氯化铵溶液中滴加适量氨水,至溶液呈中性,则c(Cl-) c(NH4+)(填“>”、“=”、“<”)。(4)在25℃下,某浓度Na2CO3溶液中由水电离出来c(OH-)=1×10-6 mol/L,则此溶液的PH值为
1)酸, pH <7,抑制
(2)PH >7 ,CH3COO- + H2O CH3COOH+OH-,Al2O3
CH3COOH+OH-,Al2O3
(3)c(Cl-) = c(NH4+)。
(4)8
(2)PH >7 ,CH3COO- + H2O
 CH3COOH+OH-,Al2O3
CH3COOH+OH-,Al2O3(3)c(Cl-) = c(NH4+)。
(4)8
试题分析:(1)中,AgNO3为强酸弱碱盐,水解后呈酸性,常温时的pH<7,溶于较浓的硝酸是为了抑制其水解;(2)中,醋酸钠为强奸弱酸盐,水解后呈碱性,常温时的PH >7,其离子方程式表示为:CH3COO- + H2O
 CH3COOH+OH-,AlCl3为强酸弱碱盐,水解后呈酸性,将AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是Al2O3,(3)中,溶液呈中性,根据电荷守恒可知道c(Cl-) = c(NH4+);(4)Na2CO3溶液程碱性,当在25℃下,由水电离出来c(OH-)=1×10-6 mol/L,则由c(H+)=1×10-8 mol/L,故PH=8。
CH3COOH+OH-,AlCl3为强酸弱碱盐,水解后呈酸性,将AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是Al2O3,(3)中,溶液呈中性,根据电荷守恒可知道c(Cl-) = c(NH4+);(4)Na2CO3溶液程碱性,当在25℃下,由水电离出来c(OH-)=1×10-6 mol/L,则由c(H+)=1×10-8 mol/L,故PH=8。点评:本题考查了盐类水解,计算PH,是高考的常考题型,本题比较基础,学生很容易得高分。

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
 :10
:10

 :10
:10 )>c(SO
)>c(SO )>c(H2SO3)
)>c(H2SO3)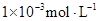 的氨水
的氨水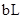 ②
②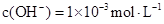 的氨水cL
的氨水cL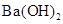 的溶液
的溶液