题目内容
某温度下,0.1mol·L-1NaHCO3溶液pH=10,下列判断正确的是( )
| A.溶液中碳酸氢根电离的氢离子浓度为10-10mol·L-1 |
B.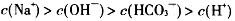 |
| C.溶液中水电离的氢氧根离子浓度为10-4mol·L-1 |
D.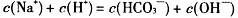 |
C
试题分析:A项:碳酸氢根离子水解大于电离,才呈碱性,H+主要由水电离生成的,溶液中总的氢离子浓度为10-10mol·L-1,故错;B项:OH-离子是由水解生成的,浓度很小,故错;D项:溶液中负电荷还有CO32-,故错。故选C。
点评:本题考查的是水溶液中,各个离子之间浓度的关系,题目难度适中,注意基础知识的学习及应用。

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
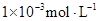 的氨水
的氨水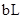 ②
②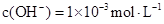 的氨水cL
的氨水cL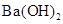 的溶液
的溶液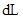
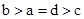
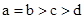
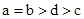
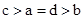
 H++OH—,在不同的温度下,其平衡常数K(25℃)=1×10-14, K(35℃)=2.1×10-14,则下列叙述正确的是:
H++OH—,在不同的温度下,其平衡常数K(25℃)=1×10-14, K(35℃)=2.1×10-14,则下列叙述正确的是: