题目内容
【题目】已知反应:3Cu +8HNO3(稀)= 3Cu(NO3)2 +2NO↑+4H2O,现有3.2g铜和足量的稀硝酸完全反应,则:
(1)产生气体在标准状况下的体积是多少?_____________
(2)将所得溶液加水配成200mL溶液,则溶液中溶质的物质的量浓度是多少?_____________
【答案】 0.75L 0.25 mol·L-1
【解析】(1)3.2g铜的物质的量是3.2g÷64g/mol=0.05mol,根据方程式可知产生气体在标准状况下的体积是![]() ;(2)根据铜原子守恒可知生成硝酸铜是0.05mol,则将所得溶液加水配成200mL溶液,溶液中溶质的物质的量浓度是0.05mol÷0.2L=0.25mol/L。
;(2)根据铜原子守恒可知生成硝酸铜是0.05mol,则将所得溶液加水配成200mL溶液,溶液中溶质的物质的量浓度是0.05mol÷0.2L=0.25mol/L。

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
【题目】已知:CH3CH2CH2CH2OH ![]() CH3CH2CH2CHO 利用如图装置用正丁醇合成正丁醛.相关数据如表:
CH3CH2CH2CHO 利用如图装置用正丁醇合成正丁醛.相关数据如表:
物质 | 沸点/℃ | 密度/(gcm﹣3) | 水中溶解性 |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
下列说法中,不正确的是( )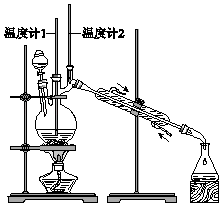
A.为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中
B.当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物
C.反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D.向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇