题目内容
【题目】已知漂白粉与浓盐酸反应产生氯气。反应方程式为:
Ca(ClO)2+4HCl(浓)CaCl2+2Cl2↑+2H2O,
某同学为了测定氯气的体积并验证干燥氯气无漂白性,现有如图装置,请回答:
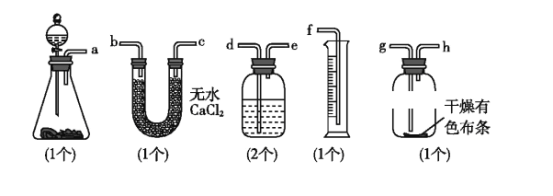
(1)请用字母填写装置的连接顺序:a接d、e接b、c接__、__接__、__接f。
(2)洗气瓶中所装液体是_______。
(3)在制氯气前,必须进行的一项操作步骤是_________________。
【答案】ghed饱和食盐水检查装置的气密性
【解析】
(1)连接仪器装置的题目一般顺序为:发生装置→净化装置→性质验证装置→气体测量或尾气处理装置。连接顺序:a接d、e接b、c接g、h接e、d接f;
(2)Cl2在饱和食盐水中的溶解度小(有时也用水代替),可除去Cl2中混有的HCl(要在Cl2干燥之前),然后通过无水CaCl2得干燥的Cl2。故洗气瓶中所装液体是饱和食盐水;
(3)任何气体的制备实验开始之前,都必须进行气密性的检验。在制氯气前,必须进行的一项操作步骤是检查装置的气密性。

【题目】第四周期过渡元素常与H2O、NH3等形成配合物。
(1)写出Fe元素基态原子的价层电子排布式_______;
(2)C、N、O元素的第一电离能从大到小的顺序为___(用元素符号表示);
(3)向盛有硫酸铜水溶液的试管里加入过量氨水,得到蓝色溶液,铜离子形成了配位数为4的配离子,写出该配离子的结构式为______。
(4)由C、H、O、S中任两种元素构成甲、乙、丙三种分子,所含原子的数目依次为3、4、8,都含有18个电子。甲和乙的主要物理性质比较如下:
熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
甲 | 187 | 202 | 2.6 |
乙 | 272 | 423 | 以任意比互溶 |
①甲分子的电子式为_________,分子构型为___________;
②1 mol乙分子含有___个σ键;
③丙分子的中心原子采取_______杂化轨道;
④甲和乙的相对分子质量基本相同,造成上述物理性质差异的主要原因是 ____________(结合具体物质解释)。







