题目内容
短周期主族元素X、Y、Z、W的原子序数依次增大,其中X、Y、Z位于不同周期,Y是形成化合物种类最多的元素,W2+与Ne原子具有相同的电子层结构.
(1)由X、Y组成的最简单化合物可作某一燃料电池的______极反应物.
(2)Z与氧组成的某种化合物可作为潜水员的供氧剂,该化合物中含有的化学键是______.
(3)即热饭盒中,有W的单质与铁粉、固体食盐组成混合物A,使用时将水加入A中,几分钟后饭菜变热了.从能量转化角度看,该过程是化学能转化为______能.写出W与水反应的化学方程式:______.
(4)500℃时,密闭容器中充入1mol/L CO2和3mol/L H2发生反应:CO2(g)+3H2(g)
CH3OH(g)+H2O(g),测得有关数据如下:
500℃时该反应的平衡常数K=______(保留一痊小数),平衡时CO2的转化率为______,温度升高,K值增大,则正反应为______热反应(填“吸”或“放”).
(5)已知:298K时,Ca(s)=Ca2+(g)+2e-△H=1807kJ/mol
O2(g)++2e-=O2-(g)△H=986kJ/mol
Ca2+(g)+O2-(g)=CaO(s)△H=-3528.5kJ/mol
298K时,金属钙和氧气反应生成CaO固体的热化学方程式为______.
(1)由X、Y组成的最简单化合物可作某一燃料电池的______极反应物.
(2)Z与氧组成的某种化合物可作为潜水员的供氧剂,该化合物中含有的化学键是______.
(3)即热饭盒中,有W的单质与铁粉、固体食盐组成混合物A,使用时将水加入A中,几分钟后饭菜变热了.从能量转化角度看,该过程是化学能转化为______能.写出W与水反应的化学方程式:______.
(4)500℃时,密闭容器中充入1mol/L CO2和3mol/L H2发生反应:CO2(g)+3H2(g)
| 加热、加压 |
| 催化剂 |
| 反应时间/min | 3 | 5 | 7 | 10 | 13 |
| c(CO2)/mol?L-1 | 0.50 | 0.37 | 0.30 | 0.25 | 0.25 |
(5)已知:298K时,Ca(s)=Ca2+(g)+2e-△H=1807kJ/mol
| 1 |
| 2 |
Ca2+(g)+O2-(g)=CaO(s)△H=-3528.5kJ/mol
298K时,金属钙和氧气反应生成CaO固体的热化学方程式为______.
Y是形成化合物种类最多的元素,应为C元素,对应的化合物种类繁多,X、Y、Z位于不同周期,且X、Y、Z、W的原子序数依次增大,则X应为H元素,Z为第三周期元素,W2+与Ne原子具有相同的电子层结构,应为Mg元素,则Z应为Na元素,则
(1)X、Y组成的最简单化合物为CH4,可被氧化,作原电池的负极,故答案为:负;
(2)Z与氧组成的化合物中能作供氧剂的为Na2O2,为离子化合物,含有离子键和共价键,
故答案为:离子键和共价键;
(3)W的单质与铁粉、固体食盐组成混合物A,使用时将水加入A中,几分钟后饭菜变热了,说明反应为放热反应,在铁粉和食盐的存在条件下发生原电池反应,如是Mg和水反应,则应在加热的条件下才可,反应的化学方程式为
Mg+2H2O
Mg(OH)2+H2↑,
故答案为:热;Mg+2H2O
Mg(OH)2+H2↑;
(4)CO2(g)+3H2(g)
CH3OH(g)+H2O(g)
起始:1mol/L 3mol/L 0 0
转化:0.75mol/L 2.25mol/L 0.75mol/L 0.75mol/L
平衡:0.25mol/L 0.75mol/L 0.75mol/L 0.75mol/L
则k=
=5.3,
平衡时CO2的转化率=
×100%=75%,
温度升高,K值增大,说明平衡向正反应方向移动,则正反应为吸热反应,
故答案为:5.3; 75%; 吸;
(5)已知:①Ca(s)=Ca2+(g)+2e-△H=1807kJ/mol
②
O2(g)++2e-=O2-(g)△H=986kJ/mol
③Ca2+(g)+O2-(g)=CaO(s)△H=-3528.5kJ/mol
利用盖斯定律将①+②+③可得:Ca(s)+
O2(g)=CaO(s),
△H=1807kJ/mol+986kJ/mol+(-735.5 kJ/mol)=-735.5 kJ/mol,
所以热化学方程式为Ca(s)+
O2(g)=CaO(s)△H=-735.5 kJ/mol,
故答案为:Ca(s)+
O2(g)=CaO(s)△H=-735.5 kJ/mol.
(1)X、Y组成的最简单化合物为CH4,可被氧化,作原电池的负极,故答案为:负;
(2)Z与氧组成的化合物中能作供氧剂的为Na2O2,为离子化合物,含有离子键和共价键,
故答案为:离子键和共价键;
(3)W的单质与铁粉、固体食盐组成混合物A,使用时将水加入A中,几分钟后饭菜变热了,说明反应为放热反应,在铁粉和食盐的存在条件下发生原电池反应,如是Mg和水反应,则应在加热的条件下才可,反应的化学方程式为
Mg+2H2O
| ||
故答案为:热;Mg+2H2O
| ||
(4)CO2(g)+3H2(g)
| 加热、加压 |
| 催化剂 |
起始:1mol/L 3mol/L 0 0
转化:0.75mol/L 2.25mol/L 0.75mol/L 0.75mol/L
平衡:0.25mol/L 0.75mol/L 0.75mol/L 0.75mol/L
则k=
| 0.75×0.75 |
| 0.25×0.753 |
平衡时CO2的转化率=
| 0.75 |
| 1 |
温度升高,K值增大,说明平衡向正反应方向移动,则正反应为吸热反应,
故答案为:5.3; 75%; 吸;
(5)已知:①Ca(s)=Ca2+(g)+2e-△H=1807kJ/mol
②
| 1 |
| 2 |
③Ca2+(g)+O2-(g)=CaO(s)△H=-3528.5kJ/mol
利用盖斯定律将①+②+③可得:Ca(s)+
| 1 |
| 2 |
△H=1807kJ/mol+986kJ/mol+(-735.5 kJ/mol)=-735.5 kJ/mol,
所以热化学方程式为Ca(s)+
| 1 |
| 2 |
故答案为:Ca(s)+
| 1 |
| 2 |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
短周期主族元素X,Y,A,B,C在元素周期表的位置如图所示,A是电负性最大的元素,则下列说法不正确的是( )
| X | A | ||
| Y | C | B |
| A、原子半径由小到大的顺序为:A<B<C<Y |
| B、A、B的氢化物的沸点由低到高的顺序为:HA<HB |
| C、X、Y最高价氧化物对应的水化物的酸性由弱到强的顺序为:H2YO3<H2XO3 |
| D、B、C简单离子的还原性由弱到强的顺序为:B-<C 2- |
短周期主族元素X、Y、Z、W在元素周期表中的相对位置如表中所示.下列判断不正确的是( )
| Y | W | |
| X | Z |
| A、原子半径最大的是X |
| B、电负性最大的是W |
| C、Y、Z原子序数差为8 |
| D、氢化物最稳定的是Z |
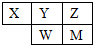 短周期主族元素X、Y、Z、W、M在元素周期表中的位置如图,W最高价氧化物对应的水化物为强酸,下列说法正确的是( )
短周期主族元素X、Y、Z、W、M在元素周期表中的位置如图,W最高价氧化物对应的水化物为强酸,下列说法正确的是( )| A、原子半径:Y<Z<M | B、M最高价氧化物对应的水化物一定是强酸 | C、Z与M对应的氢化物的沸点:M>Z | D、一定条件下,M、Y对应的单质都能与W的氢化物发生置换反应 |