籾朕坪否
17⤴壓眉倖畜液否匂嶄蛍艶割秘CH4、H2、HCl眉嶽賑悶⇧輝万断議梁業才儿膿脅屢揖扮⇧宸眉嶽賑悶議畜業⇧貫寄欺弌議乏會頁↙ ⇄| A⤴ | CH4﹅H2﹅HCl | B⤴ | CH4﹅N2﹅HCl | C⤴ | H2﹅HCl﹅CH4 | D⤴ | HCl﹅CH4﹅H2 |
蛍裂 喇PV=nRT=$\frac{m}{M}$RT⇧辛岑PM=ρRT⇧辛岑揖梁揖儿和⇧賑悶畜業岻曳吉噐凪彫櫛嵎楚岻曳⤴
盾基 盾⦿喇PV=nRT=$\frac{m}{M}$RT⇧辛岑PM=ρRT⇧辛岑揖梁揖儿和⇧賑悶畜業岻曳吉噐凪彫櫛嵎楚岻曳⇧CH4、H2、HCl眉嶽賑悶議彫櫛嵎楚蛍艶葎16g/mol、2g/mol、36.5g/mol⇧絞賑悶畜業⦿ρ↙HCl⇄﹅ρ↙CH4⇄﹅ρ↙H2⇄⇧
絞僉⦿D⤴
泣得 云籾深臥唖懸戮蟻袋協舵式凪容胎⇧廣吭功象PV=nRT尖盾唖懸戮蟻袋協舵式凪容胎⇧佃業音寄⤴

膳楼過狼双基宛
屢購籾朕
7⤴壓卑匣嶄嬬寄楚慌贋遇拝葎涙弼邑苧議卑匣頁↙ ⇄
| A⤴ | NH4+、Cu2+、SO42-、NO3- | B⤴ | K+、Ca2+、NO3-、CO32- | ||
| C⤴ | Na+、K+、HCO3-、NO3- | D⤴ | K+、MnO4-、NH4+、NO3- |
8⤴和双嗤購麗嵎議潤更才來嵎議偃峰嶄⇧危列議頁↙ ⇄
| A⤴ | 邦蛍徨岻寂狽囚議圭﨑來擬崑甥嶄邦蛍徨議均持圭塀音奉噐蛍徨畜均持 | |
| B⤴ | 喇自來囚更撹議蛍徨辛嬬頁掲自來蛍徨 | |
| C⤴ | 邦對賑、邦、甥嶄脅根狽囚 | |
| D⤴ | 蛍徨唱悶嶄匯協贋壓蛍徨寂恬喘薦⇧辛嬬贋壓慌勺囚 |
5⤴和双麗嵎侭奉窃艶音屎鳩議頁↙ ⇄
| A⤴ | 柁晒汰--冦 | B⤴ | 歓珠--珠 | C⤴ | 署奉墜--汽嵎 | D⤴ | 季君--歓昌麗 |
2⤴蝶梁業和⇧繍Cl2宥秘NaOH卑匣嶄⇧郡哘誼欺NaCl、NaClO、NaClO3議詞栽匣⇧将霞協ClO -嚥ClO3-議宣徨倖方曳葎3⦿1⇧夸Cl2嚥NaOH郡哘扮瓜珊圻議柁圻徨嚥瓜剳晒議柁圻徨議倖方曳葎↙ ⇄
| A⤴ | 21⦿5 | B⤴ | 2⦿1 | C⤴ | 4⦿1 | D⤴ | 11⦿3 |
9⤴壓炎彈彜趨和⇧和双膨嶽賑悶議購狼嶄⇧貫寄欺弌議頁↙ ⇄
〙6.72L CH4 〖3.01〜1023倖HCl蛍徨〗13.6g H2S ∠0.2mol NH3⤴
〙6.72L CH4 〖3.01〜1023倖HCl蛍徨〗13.6g H2S ∠0.2mol NH3⤴
| A⤴ | 悶持⦿∠﹅〙﹅〖﹅〗 | B⤴ | 畜業⦿〖﹅〗﹅∠﹅〙 | ||
| C⤴ | 嵎楚⦿〖﹅〗﹅〙﹅∠ | D⤴ | 狽圻徨方⦿〙﹅〖﹅〗﹅∠ |
6⤴和双嗤購麗嵎喘余議偃峰危列議頁↙ ⇄
| A⤴ | 柁賑辛喘噐徭栖邦嶧蕎 | |
| B⤴ | 40%議遮肌邦卑匣辛喘恬契遣質⇧償崙伏麗炎云 | |
| C⤴ | 垢匍焼娼辛喘噐悌夛咬喘焼 | |
| D⤴ | 炭議賑晒才匣晒麼勣頁伏撹賠準伴創⇧炭議孤蒼麼勣頁伏恢晒垢圻創 |
7⤴和双裏腺窮徨塀危列議頁↙ ⇄
| A⤴ | 柁圻徨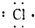 | B⤴ | 葬宣徨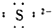 | C⤴ | 粤宣徨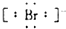 | D⤴ | 呼宣徨Ca2+ |
 ◉ 〗2-遮児-1-隷路議囚㞍塀
◉ 〗2-遮児-1-隷路議囚㞍塀 ⤴
⤴