题目内容
向10mL 0.1mol·L-1 (NH4)Al(SO4)2溶液中滴加等浓度Ba(OH)2溶液x mL。下列表述正确的是
| A.x=10时,溶液中有NH4+、Al3+、SO42-,且c(SO42-)>c(NH4+)>c(Al3+) |
| B.x=20时溶液导电能力比x=15时溶液导电能力强 |
| C.x=25时,溶液中主要有Ba2+、AlO2-,c(Ba2+)>c(AlO2-) |
| D.x=30时的离子方程式:NH4++Al3++2SO42-+2Ba2++5OH-→AlO2-+2BaSO4↓+NH3?H2O+2H2O |
AD
解析试题分析:根据题意,可得相关溶液和沉淀相关图像,a=10, a=15,a=20;
0→a,2Al3++3SO42-+3Ba2++6OH— = 2Al(OH)3↓+3BaSO4↓ 生成氢氧化铝沉淀和硫酸钡沉淀;a→b,SO42-+2NH4++2OH-+ Ba2+=2NH3·H2O+ BaSO4↓;b→c Al(OH)3+OH-=AlO2-+2H2O氢氧化铝溶解;b点为沉淀最大值,相关反应:NH4Al(SO4)2+ 2Ba(OH)2="2" BaSO4↓+ Al(OH)3↓+ NH3·H2O,则此时所耗掉Ba(OH)2的溶液体积为20mL;A、当x=10时,NH4Al(SO4)2与Ba(OH)2等物质的量反应,此时OH-量不足,OH-首先与Al3+反应,与NH4+不反应,2Al3++3SO42-+3Ba2++6OH— = 2Al(OH)3↓+3BaSO4↓,所以溶液中有未参加反应的NH4+和部分剩余的Al3+存在,同时SO42-也有剩余,但此时不会有AlO2-生成,溶液中c(NH4+)>c(Al3+),故A正确;选择AD。
考点:本题考查离子方程式的有关计算、过量计算等,难度中等,清楚氢氧根离子与铵根离子、铝离子反应的先后顺序是解题的关键。

下列反应的离子方程式正确的是( )
| A.少量二氧化碳通入水玻璃中: CO2 + SiO32― + H2O = CO32―+ H2SiO3↓ |
| B.钠投入水中:Na+ H2O = Na++OH-+ H2↑ |
| C.AlCl3溶液中加入过量氨水: Al3++4OH-= AlO2-+2H2O |
D.氯气通入水中:Cl2+H2O 2H++Cl-+ClO- 2H++Cl-+ClO- |
下列离子方程式书写正确的是
| A.金属钠和水反应:Na+H2O=Na++OH-+H2↑ |
| B.澄清石灰水中加入通入少量CO2 :Ca2++2OH-+ CO2 = CaCO3↓+H2O |
| C.过氧化钠与冷水反应:2O22-+ 2H2O = 4OH-+ O2↑ |
| D.H2SO4与Ba(OH)2混合:SO42-+Ba2++H++OH-=BaSO4↓+H2O |
下列说法正确的是( )
| A.将BaSO4放入水中不能导电,所以BaSO4是非电解质 |
| B.氨溶于水得到的氨水能导电,所以氨水是电解质 |
| C.固态的离子化合物不导电,熔融态的离子化合物导电 |
| D.强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
下列离子方程式书写正确的是
| A.铁溶于稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
| B.二氧化硫与足量烧碱溶液反应:S02+20H-=S032-+H20 |
| C.醋酸溶液与氢氧化钠溶液反应:H++OH-=H20 |
D.浓盐酸与MnO2反应制Cl2:Mn02+2H++2C1- C12↑+Mn2++H20 C12↑+Mn2++H20 |
能正确表示下列反应的离子方程式的是
| A.浓盐酸与铁屑反应:2 Fe+6 H+=2 Fe3++3 H2↑ |
| B.钠与CuSO4溶液反应:2 Na+Cu2+=Cu↓+2 Na+ |
| C.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| D.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
下列图示与对应的叙述相符的是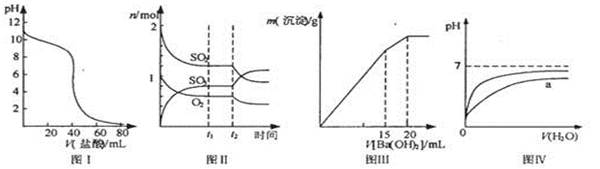
| A.图I表示盐酸滴加到0.1mol/L某碱溶液得到的滴定曲线,用已知浓度盐酸滴定未知浓度该碱时最好选取酚酞作指示剂 |
B.图II表示一定条件下进行的反应2SO2 +O2 2SO3各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积 2SO3各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积 |
| C.图III表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20mL Ba(OH)2溶液时铝离子恰好沉淀完全 |
| D.图IV表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应 的是盐酸 |
在pH=1的无色溶液中,下列各离子组因发生氧化还原反应而不能共存的是
| A.NH4+ K+ Na+ CO32- NO3- |
| B.K+ Na+ Fe2+ SO42- NO3- |
| C.NH4+ K+ Na+ HCO3-[Al(OH)4]- |
| D.NH4+ K+ Na+ NO3- I- |
向15mL 0.1mol/L Ba(OH)2溶液中,滴加等浓度NH4Al(SO4)2溶液x mL,下列叙述错误的是
| A.x=5时,溶液中有Ba2+、OH-、AlO2-,且OH-> AlO2- |
| B.x=7.5时,溶液中有NH4+、AlO2-,且NH4+=AlO2- |
| C.x=10时,溶液中有SO42-、NH4+,且H+> OH- |
| D.x=15时,溶液中有SO42-、NH4+、Al3+,且NH4+> Al3+ |