题目内容
已知Ksp[Al(OH)3]=1.3×10-33 mol4·L-4, Ksp[Fe(OH)3]=4.0×10-38 mol4·L-4。现向pH=0浓度均为0.04mol·L-1的Al3+、Fe3+溶液中加入NaOH溶液,以调节pH(设溶液体积不变),该过程中Al3+、Fe3+的浓度与pH关系正确的是( )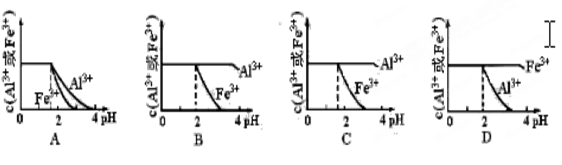
B
解析试题分析:依据已知的Ksp[Al(OH)3]=1.3×10-33 mol4·L-4、Ksp[Fe(OH)3]=4.0×10-38 mol4·L-4,可以求得Cu2+和Fe3+完全以氢氧化物沉淀时(即金属离子浓度小于10-5mol·L-1时)的pH分别为:4.7和3.2;现在向pH=0浓度均为0.04mol?L-1的Al3+、Fe3+溶液中,调节PH值,(设溶液体积不变),所以氢氧化钠溶液提高溶液PH到3.2,氢氧根离子浓度增大,使Qc大于Ksp,三价铁离子能沉淀完全,根据Ksp[Fe(OH)3]=4.0×10-38,=[Fe3+][OH-]3,计算得[OH-]=10-12mol/L;三价铁离子开始生成沉淀的PH=2,所以铁离子开始沉淀到沉淀完全的PH范围为2-3.2过程中该过程中Al3+、Fe3+的浓度与pH关系依据图象和反应原理判断,当PH=2时,铁离子开始沉淀,故B选项正确。
考点:难溶电解质的溶解平衡及沉淀转化的本质

下列有关问题,与盐的水解有关的是
① NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂
② 用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
③ 草木灰与铵态氮肥不能混合施用
④ 实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤ 加热蒸干AlCl3溶液得到Al(OH)3固体
| A.①②③ | B.②③④ | C.①④⑤ | D.①②③④⑤ |
将常温下pH=12的氢氧化钠溶液与pH=2的硫酸溶液分别加热,溶液pH的变化是
| A.前者减小后者不变 | B.前者减小后者增大 | C.都不变 | D.都减小 |
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则( )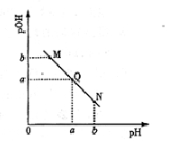
| A.M点所示溶液导电能力强于Q点 |
| B.N点所示溶液中c(CH3COO-)>c(Na+) |
| C.M点和N点所示溶液中水的电离程度相同 |
| D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
下列对于溶液中的问题叙述正确的是( )
| A.向冰醋酸中加水至配成醋酸稀溶液的过程H+的浓度逐渐减小 |
| B.在稀溶液中:H+(aq) + OH-(aq) = H2O(l); △H=-57.3kJ/mol,则含1 mol HClO的稀溶液和含1 mol KOH的稀溶液完全反应放出的热量等于57.3 kJ |
| C.常温时,pH=2的CH3COOH溶液和HCl溶液、pH=12的氨水和NaOH溶液,四种溶液中由水电离的c(H+)相等 |
| D.常温下,将稀NaOH溶液与CH3COOH溶液混合,可能出现pH>7,且c(OH-)>c(Na+)>c(H+)>c(CH3COO-)的情况 |
室温下,水的电离达到平衡:H2O H+ + OH-。下列叙述正确的是
H+ + OH-。下列叙述正确的是
| A.将水加热,平衡向正反应方向移动,Kw不变 |
| B.向水中加入少量盐酸,平衡向逆反应方向移动,c(H+)增大 |
| C.向水中加入少量NaOH固体,平衡向逆反应方向移动,c(OH-)降低 |
| D.向水中加入少量CH3COONa固体,平衡向正反应方向移动,c(OH-)= c(H+) |
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成: ① 与
与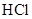 ②
②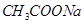 与NaOH ③
与NaOH ③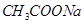 与
与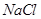 ④
④ 与
与 ,下列各项排序正确的是
,下列各项排序正确的是
| A.pH:②>③>④>① | B. :②>④>③>① :②>④>③>① |
| C.溶液中c(H+): ①>③>②>④ | D. : ①>④>③>② : ①>④>③>② |
已知一定温度下,有下列难溶电解质的相关数据:
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| KSP/250C | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不正确的是( )
A.向该混合溶液中加过量铁粉,能观察到红色固体析出
B.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
C.该混合溶液中c(SO42-):[c(Cu2+)+ c(Fe2+)+ c(Fe3+)]>5∶4
D.向该混合溶液中加入适量氯水,并调pH至3~4后过滤,能得到纯净的CuSO4溶液