题目内容
【化学-物质结构与性质】第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物.
(1)Cr的核外电子排布式为______;
(2)科学家通过X射线测得胆矾结构示意图可简单表示如下:

图中虚线表示的作用力为______;
(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4?H2O晶体.在Cu(NH3)4SO4?H2O晶体中,[Cu(NH3)4]2+ 为平面正方形结构,则呈正四面体结构的原子团是______,其中心原子的杂化轨道类型是______;
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型.试推测四羰基镍的晶体类型是______,Ni(CO)4 易溶于下列______.
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液.
【答案】分析:(1)根据核外电子排布式的书写规则书写;
(2)电子对给予-接受键被称为配位键;氢键是由已经与电负性很强的原子形成共价键的氢原子与另一个分子中电负性很强的原子之间的作用力,根据定义判断;
(3)根据价层电子对互斥理论、杂化轨道理论分析;
(4)根据其状态、熔点判断四羰基镍的晶体类型;根据相似相溶原理分析;
解答:解:(1)Cr是24号元素,其原子核外有24个电子,根据能量最低原理及洪特规则书写其核外电子排布式,3d能级的能量大于4s能级的能量,所以先排4s后排3d,轨道中的电子处于全满、半满、全空时原子最稳定,所以Cr的核外电子排布式为
1s22s22p63s23p63d54s1.
故答案为:1s22s22p63s23p63d54s1.
(2)通过图象知,图中虚线表示的作用力有铜离子和水分子之间的配位键,氢原子和另一分子中氧原子之间的氢键.
故答案为:氢键、配位键.
(3)SO42一离子中含有4个δ键,孤电子对数=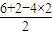 =0,所以SO42一为正四面体结构;杂化轨道数=中心原子的孤电子对数+中心原子的δ键个数,所以采用sp3杂化.
=0,所以SO42一为正四面体结构;杂化轨道数=中心原子的孤电子对数+中心原子的δ键个数,所以采用sp3杂化.
故答案为:SO42一,sp3.
(4)Ni(CO)4是液态挥发性物质,所以其熔点较低,故为分子晶体;呈正四面体构型,是对称结构,所以是非极性物质,根据相似相溶原理知,Ni(CO)4 易溶于非极性溶剂,苯、四氯化碳是非极性物质,所以Ni(CO)4 易溶于苯、四氯化碳.
故选BC.
点评:本题考查较为综合,涉及电子排布式、分子的立体构型、杂化轨道类型、氢键、化学键类型等知识,具有一定的难度,本题注意Cr原子核外电子排布式中3d上5个电子4s上1个电子,不是3d上4个电子4s上2个电子,要注意Cr、Cu原子核外电子排布式的书写.
(2)电子对给予-接受键被称为配位键;氢键是由已经与电负性很强的原子形成共价键的氢原子与另一个分子中电负性很强的原子之间的作用力,根据定义判断;
(3)根据价层电子对互斥理论、杂化轨道理论分析;
(4)根据其状态、熔点判断四羰基镍的晶体类型;根据相似相溶原理分析;
解答:解:(1)Cr是24号元素,其原子核外有24个电子,根据能量最低原理及洪特规则书写其核外电子排布式,3d能级的能量大于4s能级的能量,所以先排4s后排3d,轨道中的电子处于全满、半满、全空时原子最稳定,所以Cr的核外电子排布式为
1s22s22p63s23p63d54s1.
故答案为:1s22s22p63s23p63d54s1.
(2)通过图象知,图中虚线表示的作用力有铜离子和水分子之间的配位键,氢原子和另一分子中氧原子之间的氢键.
故答案为:氢键、配位键.
(3)SO42一离子中含有4个δ键,孤电子对数=
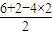 =0,所以SO42一为正四面体结构;杂化轨道数=中心原子的孤电子对数+中心原子的δ键个数,所以采用sp3杂化.
=0,所以SO42一为正四面体结构;杂化轨道数=中心原子的孤电子对数+中心原子的δ键个数,所以采用sp3杂化.故答案为:SO42一,sp3.
(4)Ni(CO)4是液态挥发性物质,所以其熔点较低,故为分子晶体;呈正四面体构型,是对称结构,所以是非极性物质,根据相似相溶原理知,Ni(CO)4 易溶于非极性溶剂,苯、四氯化碳是非极性物质,所以Ni(CO)4 易溶于苯、四氯化碳.
故选BC.
点评:本题考查较为综合,涉及电子排布式、分子的立体构型、杂化轨道类型、氢键、化学键类型等知识,具有一定的难度,本题注意Cr原子核外电子排布式中3d上5个电子4s上1个电子,不是3d上4个电子4s上2个电子,要注意Cr、Cu原子核外电子排布式的书写.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 (2011?锦州模拟)【化学--物质结构与性质】
(2011?锦州模拟)【化学--物质结构与性质】
 (2010?济南二模)【化学-物质结构与性质】
(2010?济南二模)【化学-物质结构与性质】 【化学-物质结构与性质】
【化学-物质结构与性质】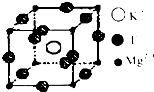 【化学--物质结构与性质】
【化学--物质结构与性质】