题目内容
某固体混合物可能由KNO3、K2SO4、KI、NaCl、CuCl2、CaCl2和Na2CO3中的一种或几种组成.依次进行下列五步实验,观察到的现象记录如下:
①混合物加水得无色透明溶液
②向上述溶液中滴加BaCl2溶液有白色沉淀生成,将该沉淀滤出,并将滤液分成两份;
③上述白色沉淀可 完全 溶于稀盐酸;
④往一份滤液中滴加氯水并加入CCl4,振荡后静置,CCl4层呈无色;
⑤往另一份滤液中加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀硝酸.
根据以上实验,
(1)可以判断出混合物中肯定含有
(2)但不能判断出是否含有
(3)为确证混合物的组成,还须做
①混合物加水得无色透明溶液
②向上述溶液中滴加BaCl2溶液有白色沉淀生成,将该沉淀滤出,并将滤液分成两份;
③上述白色沉淀可 完全 溶于稀盐酸;
④往一份滤液中滴加氯水并加入CCl4,振荡后静置,CCl4层呈无色;
⑤往另一份滤液中加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀硝酸.
根据以上实验,
(1)可以判断出混合物中肯定含有
Na2CO3
Na2CO3
;(2)但不能判断出是否含有
NaCl KNO3
NaCl KNO3
;(3)为确证混合物的组成,还须做
焰色反应和检验氯离子
焰色反应和检验氯离子
实验.分析:针对每步实验的现象分析判断,①向混合物中加入适量水全部溶解,溶液无色透明,说明一定不会含有CuCl2,不含有不溶物或反应生成不溶物;
②向步骤①溶液中滴加过量BaCl2溶液生成白色沉淀,则说明该白色沉淀是碳酸钡或是硫酸钡中的至少一种;
③取步骤②的白色沉淀,加入稀盐酸白色沉淀全部消失,说明该沉淀不会是硫酸钡,所以一定是碳酸钡;
④往一份滤液中滴加氯水并加入CCl4,振荡后静置,CCl4层呈无色,则一定没有碘单质生成,所以可以确定KI一定不存在;
⑤另一份滤液中加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀硝酸,说明该白色沉淀一定是氯化银,但无法证明该溶液中的氯离子,是来自于原混合物还是②中加入的氯化钡所致,据此分析解答即可.
②向步骤①溶液中滴加过量BaCl2溶液生成白色沉淀,则说明该白色沉淀是碳酸钡或是硫酸钡中的至少一种;
③取步骤②的白色沉淀,加入稀盐酸白色沉淀全部消失,说明该沉淀不会是硫酸钡,所以一定是碳酸钡;
④往一份滤液中滴加氯水并加入CCl4,振荡后静置,CCl4层呈无色,则一定没有碘单质生成,所以可以确定KI一定不存在;
⑤另一份滤液中加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀硝酸,说明该白色沉淀一定是氯化银,但无法证明该溶液中的氯离子,是来自于原混合物还是②中加入的氯化钡所致,据此分析解答即可.
解答:解:①向混合物中加入适量水全部溶解,溶液无色透明,说明一定不会含有不溶物或反应生成不溶物,所以可知该物质中一定不存在氯化铜;
②向步骤①溶液中滴加过量BaCl2溶液生成白色沉淀,则说明该白色沉淀可能是碳酸钡或硫酸钡,所以该物质中可能含有硫酸钾和碳酸钠;
③取步骤②的白色沉淀,加入稀盐酸白色沉淀全部消失,说明该沉淀不会是硫酸钡,所以一定是碳酸钡,故原物质中一定含有碳酸钠,从而可知该物质中一定不会含有硫酸钾,一定不会含有氯化钙,因为氯化钙能与碳酸钠反应生成碳酸钙沉淀,这与①的现象不符;
④往一份滤液中滴加氯水并加入CCl4,振荡后静置,CCl4层呈无色,则一定没有碘单质生成,所以可以确定KI一定不存在;
⑤一份滤液中加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀硝酸,说明该白色沉淀一定是氯化银,但无法证明该溶液中的氯离子,是来自于原混合物还是②中加入的氯化钡所致,
综上可得混合物中肯定含有碳酸钠,一定不含有K2SO4、KI、CuCl2、CaCl2,可能含有NaCl、KNO3.
(1)根据步骤③可以确定混合物中肯定含有碳酸钠,故答案为:Na2CO3;
(2)混合物中肯定含有碳酸钠,一定不含有K2SO4、KI、CuCl2、CaCl2,对于是否含有NaCl、KNO3不能确定,
故答案为:NaCl、KNO3;
(3)在溶液中钠离子、钾离子的检验常采用焰色反应的方法,氯离子是否存在不能确定,还需要做实验来检验,
故答案为:焰色反应和检验氯离子.
②向步骤①溶液中滴加过量BaCl2溶液生成白色沉淀,则说明该白色沉淀可能是碳酸钡或硫酸钡,所以该物质中可能含有硫酸钾和碳酸钠;
③取步骤②的白色沉淀,加入稀盐酸白色沉淀全部消失,说明该沉淀不会是硫酸钡,所以一定是碳酸钡,故原物质中一定含有碳酸钠,从而可知该物质中一定不会含有硫酸钾,一定不会含有氯化钙,因为氯化钙能与碳酸钠反应生成碳酸钙沉淀,这与①的现象不符;
④往一份滤液中滴加氯水并加入CCl4,振荡后静置,CCl4层呈无色,则一定没有碘单质生成,所以可以确定KI一定不存在;
⑤一份滤液中加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀硝酸,说明该白色沉淀一定是氯化银,但无法证明该溶液中的氯离子,是来自于原混合物还是②中加入的氯化钡所致,
综上可得混合物中肯定含有碳酸钠,一定不含有K2SO4、KI、CuCl2、CaCl2,可能含有NaCl、KNO3.
(1)根据步骤③可以确定混合物中肯定含有碳酸钠,故答案为:Na2CO3;
(2)混合物中肯定含有碳酸钠,一定不含有K2SO4、KI、CuCl2、CaCl2,对于是否含有NaCl、KNO3不能确定,
故答案为:NaCl、KNO3;
(3)在溶液中钠离子、钾离子的检验常采用焰色反应的方法,氯离子是否存在不能确定,还需要做实验来检验,
故答案为:焰色反应和检验氯离子.
点评:在解此类题时,首先分析题中的现象物质之间的关系,然后根据现象推出可以确定存在或不存在的物质,对于现象不能确定的只能再设计实验进行验证.

练习册系列答案
相关题目
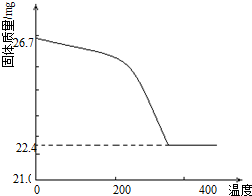 (2012?安徽)工业上从废铅酸电池的铅膏回收铅的过程中,可用碳酸盐溶液与铅膏(主要成分为PbSO4)发生反应:PbSO4(s)+CO32-(aq)?PbCO3(s)+SO42-(aq).某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分.
(2012?安徽)工业上从废铅酸电池的铅膏回收铅的过程中,可用碳酸盐溶液与铅膏(主要成分为PbSO4)发生反应:PbSO4(s)+CO32-(aq)?PbCO3(s)+SO42-(aq).某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分. 2KNO2+O2↑
2KNO2+O2↑ 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑ 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑