题目内容
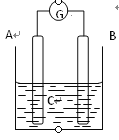
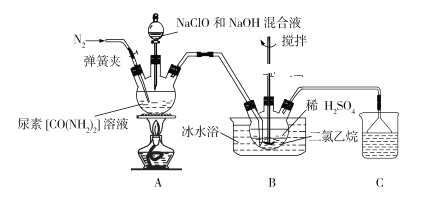
【题目】某高中科研小组模拟工业尿素法生产肼(N2H4),具体方法:先将尿素、次氯酸钠和氢氧化钠溶液混合,然后在催化剂存在的条件下反应制得肼,利用氮气吹出混合物中的肼,并用硫酸吸收制备硫酸肼。具体实验原理图如下:
已知:①肼极易溶于水,长期暴露在空气中或短时间受高温作用会爆炸分解。
②硫酸肼(N2H4·H2SO4)是类似于NH4HSO4的盐类,白色固体,微溶于冷水,易溶于热水,不溶于乙醇和二氯乙烷等有机溶剂。
③密度:ρ硫酸肼>ρ二氯乙烷>ρ稀硫酸
(1)盛装尿素溶液的装置名称为_____________________;硫酸肼的水溶液中含有多种阳离子,其中阳离子N2H5+的电子式为________________________。
(2)反应前应先通入一段时间氮气,其目的为________________________________。
(3)装置A中发生反应制备肼的离子方程式为_______________________________。
(4)装置B中二氯乙烷的作用为__________________________________________;使用冰水浴的作用__________________________________________________。
(5)装置B反应完全后需经过过滤、洗涤、干燥等操作得到硫酸肼,洗涤过程中最好选择下列那种洗涤剂________________(填字母)。
A.冷水 B.热水 C.无水乙醇 D.饱和食盐水
(6)若实验中所用的NaClO和NaOH混合液中两溶质的浓度均为0.1mol·L1,则此溶液中离子浓度的大小顺序为______________________________________。
【答案】三颈烧瓶 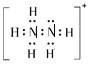 赶走装置中的空气,避免空气与肼反应 ClO+2OH+CO(NH2)2
赶走装置中的空气,避免空气与肼反应 ClO+2OH+CO(NH2)2![]() N2H4+Cl+
N2H4+Cl+![]() +H2O 防倒吸,同时使产物硫酸肼脱离反应混合液 利于产物析出,同时降温防爆炸 C c(Na+)>c(OH)>c(ClO)>c(H+)
+H2O 防倒吸,同时使产物硫酸肼脱离反应混合液 利于产物析出,同时降温防爆炸 C c(Na+)>c(OH)>c(ClO)>c(H+)
【解析】
(1)盛装尿素溶液的装置名称为三颈烧瓶;硫酸肼的水溶液中含有多种阳离子,其中阳离子N2H5+可以认为由N2H4与H+通过配位键结合,在N2H4中,每个N原子与两个H原子形成共价键,则两个N原子间还应形成一对共用电子。
(2)反应前应先通入一段时间氮气,其目的为排尽装置内的空气,防止空气与肼反应。
(3)装置A中,碱性溶液,ClO在催化剂作用下,将CO(NH2)2氧化为N2H4,自身被还原为Cl,同时生成![]() 和H2O。
和H2O。
(4)装置B中二氯乙烷的作用为防倒吸,同时使产物硫酸肼脱离反应混合液;使用冰水浴的作用是降低产物的溶解度,同时降温防爆。
(5)装置B反应完全后需经过滤、洗涤、干燥等操作得到硫酸肼,洗涤过程中尽可能减少产品的溶解损失,所以最好选择无水乙醇。
(6)若实验中所用的NaClO和NaOH混合液中两溶质的浓度均为0.1mol·L1, c(Na+)=0.1mol·L1,因水解c(ClO)<0.1mol·L1,c(OH)>0.1mol·L1,由此可确定溶液中离子浓度的大小。
(1)盛装尿素溶液的装置名称为三颈烧瓶;N2H5+可以认为由N2H4与H+通过配位键结合,在N2H4中,每个N原子与两个H原子形成共价键,则两个N原子间还应形成一对共用电子,电子式为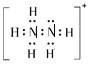 。答案为:三颈烧瓶;
。答案为:三颈烧瓶;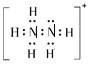 ;
;
(2)反应前应先通入一段时间氮气,其目的为排尽装置内的空气,防止空气与肼反应。答案为:赶走装置中的空气,避免空气与肼反应;
(3)装置A中,碱性溶液,ClO在催化剂作用下,将CO(NH2)2氧化为N2H4,自身被还原为Cl,同时生成![]() 和H2O,反应方程式为ClO+2OH+CO(NH2)2
和H2O,反应方程式为ClO+2OH+CO(NH2)2![]() N2H4+Cl+
N2H4+Cl+![]() +H2O。答案为:ClO+2OH+CO(NH2)2
+H2O。答案为:ClO+2OH+CO(NH2)2![]() N2H4+Cl+
N2H4+Cl+![]() +H2O;
+H2O;
(4)装置B中二氯乙烷的作用为防倒吸,同时使产物硫酸肼脱离反应混合液;使用冰水浴的作用是降低产物的溶解度,同时降温防爆。答案为:防倒吸,同时使产物硫酸肼脱离反应混合液;利于产物析出,同时降温防爆炸;
(5)装置B反应完全后需经过滤、洗涤、干燥等操作得到硫酸肼,洗涤过程中尽可能减少产品的溶解损失,所以最好选择无水乙醇。答案为:C;
(6)若实验中所用的NaClO和NaOH混合液中两溶质的浓度均为0.1mol·L1,c(Na+)=0.1mol·L1,因水解c(ClO)<0.1mol·L1,c(OH)>0.1mol·L1,由此可确定溶液中离子浓度的关系为:c(Na+)>c(OH)>c(ClO)>c(H+)。答案为:c(Na+)>c(OH)>c(ClO)>c(H+)。

【题目】下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)
A | B | C | D |
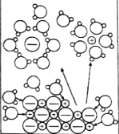
NaCl溶于水 |
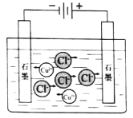
电解CuCl2溶液 |
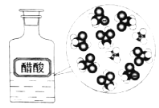
CH3COOH在水中电离 |
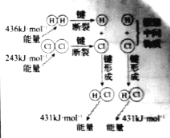
H2与Cl2反应能量变化 |
NaCl | CuCl2 | CH3COOH | H2(g)+Cl2(g) ΔH=183kJ·mol1 |
A. AB. BC. CD. D