题目内容
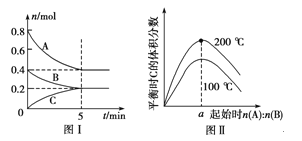
【题目】在容积为2 L的恒容密闭容器中发生反应xA(g)+yB(g)![]() zC(g),图Ⅰ表示200 ℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是 ( )
zC(g),图Ⅰ表示200 ℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是 ( )
A.图Ⅱ所知反应xA(g)+yB(g)![]() zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2
B.200 ℃时,反应从开始到平衡的平均速率v(B)=0.02 mol·L-1·min-1
C.若在图Ⅰ所示的平衡状态下,再向体系中充入He的瞬间,v正>v逆
D.200 ℃时,向容器中充入2 mol A和1 mol B,达到平衡时,A的体积分数等于0.5
【答案】B
【解析】
试题分析:A.由图像可知:升高温度,平衡时C的体积分数增大,说明升高温度化学平衡向正反应方向移动,根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动,则正反应方向为吸热反应。所以△H>0,根据图Ⅰ所示可知该反应的方程式为2A+B![]() C,只有当两种反应物按照方程式的计量数的关系加入时生成物C达到平衡时含量才会最高,则a=2,A错误;B.200℃时,反应从开始到平衡的平均速率v(B)={(0.4-0.2) mol÷2 L}÷5 min=0.02 mol/(L·min),B正确;C.若在图Ⅰ所示的平衡状态下,再向体系中充入He,由于平衡混合物中各组分的浓度没变,所以平衡不移动,v(正)=v(逆),C错误;D.由图Ⅰ可知在200℃时,若加入0.8mol A和0.4mol B,达到平衡时A的含量为0.5。若向容器中充入2 mol A 和1 mol B,即增大了反应物的浓度,同时容器内气体的压强增大。根据平衡移动原理:增大压强,化学平衡向正反应方向移动。所以达到平衡时,A 的体积分数小于0.5,D错误;答案选B。
C,只有当两种反应物按照方程式的计量数的关系加入时生成物C达到平衡时含量才会最高,则a=2,A错误;B.200℃时,反应从开始到平衡的平均速率v(B)={(0.4-0.2) mol÷2 L}÷5 min=0.02 mol/(L·min),B正确;C.若在图Ⅰ所示的平衡状态下,再向体系中充入He,由于平衡混合物中各组分的浓度没变,所以平衡不移动,v(正)=v(逆),C错误;D.由图Ⅰ可知在200℃时,若加入0.8mol A和0.4mol B,达到平衡时A的含量为0.5。若向容器中充入2 mol A 和1 mol B,即增大了反应物的浓度,同时容器内气体的压强增大。根据平衡移动原理:增大压强,化学平衡向正反应方向移动。所以达到平衡时,A 的体积分数小于0.5,D错误;答案选B。

【题目】氯化亚铜广泛应用于有机合成。工业上以低品位铜矿(主要含CuS、Fe2O3、SiO2)为原料,制备氯化亚铜的生产工艺如下:
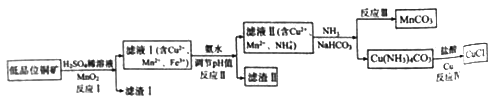
(1)CuS中Cu的化合价为_____________。
(2)滤渣Ⅰ的成分除S之外还有__________,反应Ⅰ中MnO2的作用是______________
(3)已知生成氢氧化物的pH如下表:
沉淀物 | Fe(OH)3 | Mn(OH)2 | Cu(OH)2 |
开始沉淀的pH | 2.7 | 8.3 | 4.2 |
完全沉淀的pH | 3.2 | 9.8 | 6.7 |
则反应Ⅱ中用氨水调节pH值的范围是________________。
(4)检验滤液Ⅱ中是否含有Fe3+的试剂是____________。
(5)请用化学用语回答:
①反应中Ⅲ生成难溶MnCO3的离子方程式_____________;
②反应Ⅳ素所对应的化学方程式____________________。
(6)氯化亚铜的定量分析:
步骤Ⅰ.称取0.2500g的样品和10.0mL 1.0mol/L的FeCl3溶液置于250mL锥形瓶中,不断摇动;
步骤Ⅱ.待样品溶解后,加水10.0mL和3滴指示剂;
步骤Ⅲ.用0.1000mol/L CeOSO4标准溶液滴至终点,并记录读数。重复实验两次,测得数据如下:
序号 | 1 | 2 | 3 |
起始读数 | 0.95mL | 0.70mL | 1.00mL |
终点读数 | 20.95mL | 24.95mL | 21.00mL |
已知:CuCl+FeCl3=CuCl2+FeCl2 Fe2++Ce4+=Fe3++Ce3+
①数据处理:计算CuCl纯度________________;
②误差分析:下列操作会使滴定结果偏高的是__________________。
A.锥形瓶中有少量蒸馏水
B.滴定终点读数时仰视滴定管刻度线,其他操作正确
C.0.1000mol/L CeOSO4溶液久置后浓度变小
D.滴定前滴定管尖嘴有气泡,滴定后气泡消失
E.所取FeCl3溶液体积偏大