题目内容
【题目】某研究小组验证乙醇的还原性,装置如下:

(1)乙醇被氧化的产物为______________,1mol乙醇失去___________mol电子。
(2)通入乙醇反应,试管A的现象是___________;反应结束后,如果对试管B进行加热,将会出现的现象是_____________________。
(3)研究小组发现,反应后期有不溶于水的气体出现,收集该气体证明是H2,为了进一步研究设计了如下装置(部分加热仪器已省略):
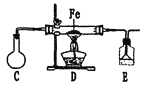
①C装置盛有的物质是_____________,先加热____________(填装置代号),赶走装置内的空气。
② E收集液体产物,甲认为是乙酸,乙认为还是乙醛,请你判断谁的推测更合理,并说明理由:________________________。
【答案】 乙醛 2 红色固体变黑 砖红色沉淀 乙醇 C 乙正确,依据氧元素守恒和得失电子,若生成乙酸则气体除了有氢气还有乙烯,这与实验现象不符,所以乙正确。
【解析】(1)乙醇在催化剂作用下被氧化的产物为乙醛,属脱氢氧化,每摩乙醇被脱去2mol氢原子,则1mol乙醇失去2mol电子;
(2)通入乙醇反应,试管A中氧化铁被还原为铁,可观察到的现象是红色固体变黑;乙醛和新制的氢氧化铜混合加热,生成砖红色Cu2O沉淀;
(3)①C装置盛有的物质是乙醇,先加热C装置,利用乙醇蒸气赶走装置内的空气;
② E收集液体产物,依据氧元素守恒和得失电子,若生成乙酸则气体除了有氢气还有乙烯,这与实验现象不符,所以产物应该是乙醛,即乙正确。

练习册系列答案
相关题目