题目内容
【题目】由徐光宪院士发起,院士学子同创的《分子共和国》科普读物最近出版了,全书形象生动地戏说了BF3、TiO2、CH3COOH、CO2、NO、二茂铁、NH3、HCN、H2S、O3、异成二烯和萜等众多“分子共和国”中的明星。
(1)写出Fe2+的核外电子排布式__________。
(2)下列说法正确的是_______。
a.H2S和O3分子的构型相同
b.BF3和NH3分子的极性相同
c.CO2、HCN分子中C原子的杂化方式相同
d.CH3COOH分子中C原子的杂化方式相同
(3)N3-与CO2分子互为等电子体,则N3-的空间构型为_______。含Co3+的配合物Co[(N3)(NH3)5]SO4中的配体是_________。
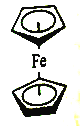
(4)二茂铁是由C5H5-和Fe2+形成的配合物,其结构如图所示。该配合物中共含有____种化学环境不同的氢。
(5)砷和氮位于同一主族,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,它们有着广泛的用途。同答下列问题:
①写出砷的价电子排布式___________。
②工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出该反应的化学方程式: ___________。
【答案】 [Ar]3d6 ac 直线型 N3-和NH3 1 4s24p3 2As2S3+5O2+6H2O=4H3AsO4+6S
【解析】(1)考查电子排布式的书写,Fe位于第四周期VIII族,Fe2+的核外电子排布式为[Ar]3d6;(2)考查杂化类型、极性分子或非极性分子的判断、空间构型的判断,a、H2S中心原子S有2个σ键,2个孤电子对,价层电子对数为4,空间构型为V型,O3的构型为V型,因此两者构型相同,故a正确;b、BF3的空间构型为平面正三角形,属于非极性分子,NH3空间构型为三角锥,属于极性分子,故b错误;c、CO2的空间构型为直线型,C的杂化类型为sp,HCN为直线型,C的杂化类型为sp,故c正确;d、-CH3中C的杂化类型为sp3,-COOH中C的杂化类型为sp2,故d错误;(3)考查空间构型的判断、配合物的组成,等电子体具有相似的化学键特征,空间构型相似,CO2为直线型,则N3-的空间构型为直线型;根据配合物的组成,N3-和NH3为配体;(4)考查等效氢的判断,根据结构,此结构属于对称结构,因此只有1种化学环境的氢原子;(5)考查价电子、化学方程式的计算,①As位于第四周期VA族,As的价电子排布式为4s24p3;②反应物有As2S3、H2O、O2,产物有H3AsO4和S,因此反应方程式为2As2S3+5O2+6H2O=4H3AsO4+6S。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案【题目】由下列实验及现象不能推出相应结论的是
实验 | 现象 | 结论 | |
A | 向2mL0.1mol·L-1的FeCl3溶液中加足量铁粉,振荡,加1滴KSCN溶液 | 黄色逐期消失,加KSCN溶液颜色不变 | 还原性:Fe>Fe2+ |
B | 将金属钠在燃烧匙中点燃,迅速伸入集满CO2的集气瓶 | 集气瓶中产生大量白烟,瓶内有黑色颗粒产生 | CO2具有氧化性 |
C | 加热盛有少NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3显碱性 |
D | 向2支盛有2mL相同浓度银氨溶液的试管中分别加入2滴相同浓度的NaCl和NaI溶液 | 一只试管中产生黄色沉淀,另一支中无明显现象 | Ksp(AgI)<Ksp(AgCl) |
A. A B. B C. C D. D
【题目】氧族元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解。
(1)下面曲线表示卤族元素某种性质随核电荷数的变化趋势。正确的是_______。

(2)溴化碘(IBr)的化学性质类似于卤素单质,溴化碘和水反应所得产物中有一种为三原子分子,该分子的电子式为_______。
(3)F2与其他卤素单质反应可以生成CF3、BrF3等。已知反应Cl2(g)+3F2(g)=2C1F3(g)△H=-313kJ/mo1;F-F键的键能为159 kJ/mo1;,Cl-C1键的键能为242 kJ/mo1;则ClF3中C1-F键的平均健能为____kJ/mol。ClF3的熔、沸点比BrF3的______(填“高”或“低”)。
(4)根据第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是______。
氟 | 氯 | 溴 | 碘 | |
第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(5)无机含氧酸HmROn可以写成(HO)mROn-m的形式,(n-m)的值越大,HmROn的酸性越强。则酸性:H2SeO4_____H2SeO3(填“<”或“>”)。
(6)S的常见单质S8的结构为![]() ,S原子的轨道杂化方式是______。
,S原子的轨道杂化方式是______。
(7)一定条件下,CH4和CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体。CH4与H2O形成的水合物俗称“可燃冰”。“可燃冰“中存在的分子间作用力是_______。

【题目】碳、氮及其化合物在工农业生产生活中有着重要作用。请回答下列问题:
(1)汽车尾气中的处理NO的方法也可用H2将NO还原为N2。
已知: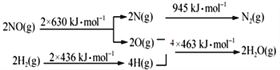
H2还原NO生成氮气和水蒸气的热化学方程是_______________________________。
(2)高炉炼铁产生的高炉气中含有CO、H2、CO2等气体,利用CO和H2在催化剂作用下合成甲醇,是减少污染、节约能源的一种新举措,反应原理为CO(g)+2H2(g)![]() CH3OH(g) ΔH。在体积不同的两个恒容密闭容器中分别充入1molCO和2mol H2,测得平衡混合物中CH3OH 的体积分数在不同压强下随温度的变化如图。
CH3OH(g) ΔH。在体积不同的两个恒容密闭容器中分别充入1molCO和2mol H2,测得平衡混合物中CH3OH 的体积分数在不同压强下随温度的变化如图。
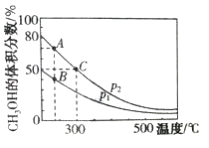
①上述合成甲醇的反应是__________________(填“吸热”或“放热”)反应,图像中的压强p1、p2的大小关系是_______________,判断的理由是________________________。
②从上图A、B、C三点中选填下表物理量对应最大的点(用“A”、“B”或“C”填写)。
反应速率V | 平衡常数K | 平衡转化率a |
____________ | _____________ | _____________ |
③在300℃时,向C点平衡体系中再充入0.25molCO、0.5molH2和0.25molCH3OH。该平衡_________(填“向正反应方向”、“向逆反应方向”或“不”)移动。
(3)有利于提高CO平衡转化率的措施有_________________。
A.使用催化剂 B.投料比不变,增加CO的浓度
C.降低反应温度 D.通入He气体使体系的压强增大
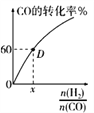
(4)一定温度下,CO的转化率与起始投料比![]() 的变化关系如图所示,测得D点氢气的转化率为40%,则x=__________________。
的变化关系如图所示,测得D点氢气的转化率为40%,则x=__________________。