题目内容
【题目】下列关于物质结构的说法不正确的是
A.在NH3和PH3分子中键长:N-H>P-H
B.晶格能:NaF>NaCl>NaBr
C.CS2的填充模型:![]()
D.CH4和NH4+都是正四面体结构,键角均为109°28′
【答案】A
【解析】
A.与同种原子形成共价键,原子半径越大,键长就越大。由于原子半径P>N,所以原子半径在NH3和PH3分子中键长:N-H<P-H,A错误;
B.元素的非金属性越强,与同种金属阳离子形成的离子化合物的离子键就越强,该物质的晶格能就越大。元素的非金属性F>Cl>Br,所以晶格能:NaF>NaCl>NaBr,B正确;
C.C原子与2个S原子形成四个共价键,三个原子在同一直线上,由于原子半径S>C,所以CS2分子的填充模型为![]() ,C正确;
,C正确;
D.CH4和NH4+的中心原子都采用sp3杂化,微粒的空间构型都是正四面体结构,键角均为109°28′,D正确;
故合理选项是A。

【题目】苯甲酸甲酯是一种重要的工业原料,有机化学中通过酯化反应原理,可以进行苯甲酸甲酯的合成。有关物质的物理性质、实验装置如下所示:
苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
熔点/℃ | 122.4 | -97 | -12.3 |
沸点/℃ | 249 | 64.3 | 199.6 |
密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
水溶性 | 微溶 | 互溶 | 不溶 |
实验一:制取苯甲酸甲酯
在大试管中加入15g苯甲酸和一定量的甲醇,边振荡边缓慢加入一定量浓硫酸,按图A连接仪器并实验。
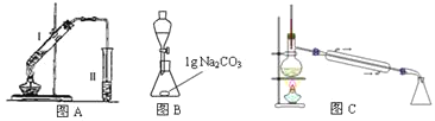
(1)苯甲酸与甲醇反应的化学方程式为_____________________________________________。
(2)大试管Ⅰ中除了装有15g苯甲酸和一定量的甲醇和一定量浓硫酸外还需要加入沸石,其作用是_______________________。
(3)中学实验室中制取乙酸乙酯时为了提高产率可以采取的措施有:(答两条措施)_______________。
实验二:提纯苯甲酸甲酯
该实验要先利用图B装置把图A中制备的苯甲酸甲酯水洗提纯,再利用图C装置进行蒸馏提纯
(4)用图B装置进行水洗提纯时,为了洗去苯甲酸甲酯中过量的酸,B装置中应加入______________。
(5)用图C装置进行蒸馏提纯时,当温度计显示_________℃时,可用锥形瓶收集苯甲酸甲酯。